题目内容
【题目】甲醇可作为燃料电池的原料,以CH4和H2O为原料,通过下列反应来制备甲醇:
CH4(g)+H2O(g)═CO(g)+3H2(g) △H=+206.0kJmol-1
CO(g)+2H2(g)═CH3OH(g) △H=-129.0kJmol-1
(1)CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为______。
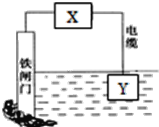
(2)甲醇对水质会造成一定污染,有一种电化学法可消除这种污染,其原理是通电后,将Co2+氧化成Co3+,然后以Co3+作氧化剂把水中的甲醇氧化成CO2而净化。实验室用如图装置模拟上述过程:

①完成除去甲醇的离子方程式:______
Co3++CH3OH+H2O═Co2++……
②若如图装置中的电源为甲醇—空气—KOH溶液的燃料电池,则电池负极的电极反应式:___。
【答案】CH4(g)+H2O(g)=CH3OH(g)+H2(g)△H=+77.0 kJ/mol 6Co3++CH3OH+H2O=CO2↑+6Co2++6H+ CH3OH-6e-+8OH-=CO32-+6H2O
【解析】
(1)依据热化学方程式和盖斯定律计算;
(2)①通电后,将Co2+氧化成Co3+,Co3+将CH3OH氧化成CO2,自身被还原成Co2+,结合电子守恒、原子守恒和电荷守恒书写离子方程式;
②甲醇在负极发生失电子的氧化反应,结合介质、守恒书写电极反应式。
(1)①CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.0kJ/mol
②CO(g)+2H2(g)=CH3OH(g)△H=-129.0 kJ/mol
根据盖斯定律,将①+②得CH4(g)+H2O(g)=CH3OH(g)+H2(g)△H=+206.0kJ/mol-(-129.0kJ/mol)=+77.0 kJ/mol,
故答案为:CH4(g)+H2O(g)=CH3OH(g)+H2(g)△H=+77.0 kJ/mol;
(2)①甲醇被氧化生成二氧化碳,Co3+被还原生成Co2+,溶液呈酸性,则生成物中含有氢离子,所以该反应离子方程式为6Co3++CH3OH+H2O=CO2↑+6Co2++6H+,
故答案为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+;
②正极上氧气得电子和水反应生成氢氧根离子,电极反应式为O2+H2O+4e-═4OH-,负极是甲醇失电子在碱溶液中生成碳酸根,故答案为:CH3OH-6e-+8OH-=CO32-+6H2O,
故答案为:CH3OH-6e-+8OH-=CO32-+6H2O。

【题目】4种相邻的主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。回答下列问题:
m | n | ||
x | y |
(1)元素x在周期表中的位置是第____。其单质可采用电解熔融的___方法制备。用电子式表示该化合物的形成过程:___。
(2)m、n、y三种元素最高价氧化物的水化物中,酸性最强的是____,碱性最强的是____。(填化学式)
(3)气体分子(mn)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式是____。