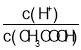题目内容
【题目】I、烟道气中的NOx是主要的大气污染物之一,为了监测其含量,选用如下检测方法。回答下列问题:将vL气样通入适量酸化的H2O2溶液中,恰好使NOx完全被氧化成NO3-,加水稀释至100.00mL。量取20.00mL该溶液,加入v1mLc1mol·L-1FeSO4标准溶液(过量),充分反应后,用c2mol·L-1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2mL。
(1)NO被H2O2氧化为NO3-的离子方程式为___。
(2)加水稀释到100.00ml所用的玻璃仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要___;滴定操作使用的玻璃仪器主要有___。
(3)滴定过程中发生下列反应:3Fe2++NO3-+4H+=NO↑+3Fe3++2H2O、Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
则气样中NOx的物质的量为___mol。
(4)下列操作会使滴定结果偏高的是___
A.滴定管未用标准液润洗
B.锥形瓶洗净后还存留少量的水
C.滴定管滴定前读数正确,滴定后俯视读数
D.FeSO4标准溶液部分变质
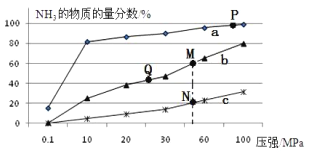
II、常温下,用酚酞作指示剂,用0.10mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol·L-1的 CH3COOH溶液和HCN溶液所得滴定曲线如图。

(已知:CH3COOH、 HCN的电离平衡常数分别为1.75×10-5、6.4×10-10)
(1)图___(a或b)是NaOH溶液滴定HCN溶液的pH变化的曲线。
(2)点③所示溶液中所含离子浓度的从大到小的顺序:___。
(3)点①和点②所示溶液中:c(CH3COO-)-c(CN-)___c(HCN)-c(CH3COOH)(填“>、<或=”)
【答案】2NO+3H2O2=2H++2NO3-+2H2O 100mL容量瓶 锥形瓶、酸式滴定管 ![]() CD a c(Na+)=c(CH3COO-)>c(H+)=c(OH-) =
CD a c(Na+)=c(CH3COO-)>c(H+)=c(OH-) =
【解析】
I、(1)NO被H2O2氧化为NO3-,N元素的化合价升高,过氧化氢中O元素的化合价降低;(2)加水稀释硝酸至100.00mL溶液时,需100mL容量瓶;滴定操作主要用到铁架台、酸式滴定管、锥形瓶等;(3)由反应结合电子守恒可知存在Cr2O72-~6Fe2+~2NO3-,以此计算;(4)误差分析的方法是把其他因素都归结到对标准溶液体积的影响上面来;
II、(1)由图象可知,V(NaOH)=0时,a曲线对应的酸的pH大于b曲线,则a曲线对应的酸的电离程度小于b曲线,结合CH3COOH、HCN的电离平衡常数大小分析解答:酸的电离平衡常数越大,酸的酸性越强,pH越小;(2)根据电荷关系判断;(3)混合溶液中存在物料守恒,点①、点②c(Na+)相同,根据物料守恒分析判断。
I、(1)NO被H2O2氧化为NO3-的离子方程式是2NO+3H2O2═2H++2NO3-+2H2O,故答案为:2NO+3H2O2═2H++2NO3-+2H2O;
(2)稀释硝酸至100.00mL溶液时,需100mL容量瓶,滴定操作主要用到铁架台、酸式滴定管、锥形瓶、其中玻璃仪器为酸式滴定管、锥形瓶,故答案为:100mL容量瓶;酸式滴定管、锥形瓶;
(3)n(Cr2O72-)=c2v2×10-3mol,由Cr2O72-~6Fe2+可知过量的Fe2+为6c2v2×10-3mol,则与量取的20.00mL溶液中NO3-反应的Fe2+为c1v1×10-3mol-6c2v2×10-3mol=(c1v1-6c2v2)×10-3mol,由3Fe2+~NO3-可知100.00mL原溶液中NO3-为![]() ×(c1v1-6c2v2)×10-3mol×
×(c1v1-6c2v2)×10-3mol×![]() =
=![]() ,故答案为:
,故答案为:![]()
(4)A、滴定管未用标准液润洗,导致消耗K2Cr2O7标准溶液体积增大,使测定剩余亚铁离子偏高,测定含N量偏低,则使NOx含量测定结果偏低,故A不选;
B、锥形瓶洗净后还存留少量的水,对整个测定结果无影响,故B不选;
C、滴定管滴定前读数正确,滴定后俯视读数,导致消耗K2Cr2O7标准溶液体积减小,使测定剩余亚铁离子偏低,由3Fe2++NO3-+4H+=NO↑+3Fe3++2H2O中测定含N量偏高,则使NOx含量测定结果偏高,故C选;
D、FeSO4标准溶液部分变质,会导致测定剩余亚铁离子偏低,3Fe2++NO3-+4H+=NO↑+3Fe3++2H2O中测定含N量偏高,则使NOx含量测定结果偏高,故D选;故答案为:CD;
II、(1)由图象可知,V(NaOH)=0时,a曲线对应的酸的pH大于b曲线,则a曲线对应的酸的电离程度小于b曲线,由酸的电离平衡常数可知:酸的电离平衡常数越大,酸的酸性越强,pH越小,所以a曲线是NaOH溶液滴定HCN溶液的pH变化的曲线,故答案为:a;
(2)溶液的电荷关系为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),点③所示溶液呈中性,c(H+)=c(OH-),所以溶液中所含离子浓度的从大到小的顺序为c(Na+)=c(CH3COO-)>c(H+)=c(OH-),故答案为:c(Na+)=c(CH3COO-)>c(H+)=c(OH-);
(3)点①和点②溶液中物料守恒得c(CH3COO-)+c(CH3COOH)=c(CN-)+c(HCN)=2c(Na+),所以有c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH),故答案为:=;