题目内容
16.根据表中维生素C的有关信息,回答下列问题| 分子式 | C6H806 |
| 物理特性 | 可口酸味 |
| 化学特性 | 还原性,易被氧化 |
| 重要功能 | 抗坏血病 |
| 主要存在 | 新鲜水果,绿色蔬菜 |
(2)维生素C是一种水溶性维生素,其水溶液显酸性(填“酸”或“碱”),服用补铁(Fe2+)制剂时医生常建议同时服用维生素C,这是因为维生素C具有还原(填“氧化”或“还原”)性;生吃新鲜蔬菜要比熟吃时维生素C的损失小,因为维生素C在受热时很容易被氧化 (填“氧化”或“还原”);
(3)维生素C对于治疗下列哪种疾病比较有效A.
A.坏血病 B.脑炎 C.骨折 D.肺炎.
分析 (1)根据食物所含的营养素种类解题;
(2)维生素C又叫L-抗坏血酸,酸性,是一种水溶性维生素,维生素C具有还原性,在空气中及高温下易被氧化;
(3)维生素C可治坏血病.
解答 解:(1)苹果、西红柿富含维生素C,薯片富含淀粉,牛肉干富含蛋白质,故答案为:苹果;西红柿;
(2)维生素C溶液呈酸性;生吃新鲜蔬菜要比熟吃时,维生素C的损失小,维生素C具有还原性,服用补铁(Fe2+)制剂时医生常建议同时服用维生素C,维生素C在空气中及高温下易被氧化,故答案为:酸;还原;氧化;
(3)维生素C又叫L-抗坏血酸,可治坏血病,故答案为:A.
点评 本题考查营养素的来源、维生素C的性质,难度不大,解答本题的关键是把握相关物质的性质,学习中注意积累.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
6.短周期主族元素A、B、C、D,原子序数依次增大.A、C的原子序数的差为8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半.下列叙述正确的是( )
| A. | 单质B常温下能溶于浓硝酸 | |
| B. | A的氢化物沸点高于C的氢化物,因为A的非金属性比C强 | |
| C. | C、D形成的化合物CD2分子中各原子都满足8电子稳定结构 | |
| D. | 元素A与C形成的化合物CA2的水溶液中通入D单质充分反应后,溶液酸性减弱 |
4.在常温常压下,等物质的量的下列物质完全燃烧,消耗氧气最多的是( )
| A. | 甲烷 | B. | 乙醇 | C. | 苯 | D. | 乙酸乙酯 |
11.mg的铜投入l00ml某浓度HNO3中,铜完全溶解,共收集到672ml NO、NO2混合气体(标准状况).向反应后的溶液中滴入100m1 8mol/L NaOH溶液时沉淀达到最大;将盛有反应生成气体的容器倒扣在水中,通入标准状况下的O2 448ml,恰好使气体完全溶于水中.则下列有关说法正确的是( )
| A. | m的值为2.56 | |
| B. | 反应之前硝酸溶液的浓度为8 mol/L | |
| C. | NO与NO2混合气中NO与NO2的体积之比为l:5 | |
| D. | 沉淀的最大质量为(m+0.8x17)g |
8.物质的量浓度都是0.1mol/L的CH3COOH和CH3COONa混合溶液,已知其中c(CH3COO-)>c(Na+),对该溶液的下列判断正确的是( )
| A. | c(H+)<c(OH-) | B. | c(CH3COOH)+c(CH3COO-)=0.2mol/L | ||
| C. | c(CH3COOH)>c(CH3COO-) | D. | c(CH3COO-)+c(OH-)=0.1mol/L |
5.下列叙述正确的是( )
| A. | 除去乙烷中少量的乙烯:通过KMnO4溶液,再用浓硫酸干燥 | |
| B. | 除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液 | |
| C. | 鉴别溴乙烷中的溴原子,可直接加入AgNO3溶液 | |
| D. | 除去乙醇中少量的水:加足量生石灰,蒸馏 |
6.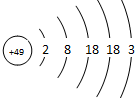 张青莲是我国著名的化学家.1991年,他准确测得In的原子量为114.818,被国际原子量委员会采用为新的标准值.这是原子量表中的首次采用我国测定的原子量值.已知In的原子结构如图所示,则下列关于In的说法不正确的是( )
张青莲是我国著名的化学家.1991年,他准确测得In的原子量为114.818,被国际原子量委员会采用为新的标准值.这是原子量表中的首次采用我国测定的原子量值.已知In的原子结构如图所示,则下列关于In的说法不正确的是( )
 张青莲是我国著名的化学家.1991年,他准确测得In的原子量为114.818,被国际原子量委员会采用为新的标准值.这是原子量表中的首次采用我国测定的原子量值.已知In的原子结构如图所示,则下列关于In的说法不正确的是( )
张青莲是我国著名的化学家.1991年,他准确测得In的原子量为114.818,被国际原子量委员会采用为新的标准值.这是原子量表中的首次采用我国测定的原子量值.已知In的原子结构如图所示,则下列关于In的说法不正确的是( )| A. | In在反应中容易失电子 | |
| B. | In为长周期元素 | |
| C. | In的最高价氧化物对应的水化物为强碱 | |
| D. | In为过渡元素 |