题目内容
5.下列过程中,共价键被破坏,不能说明有分子间作用力的存在的是( )| A. | 碘升华 | B. | HI气体受热分解 | ||
| C. | 食盐熔化 | D. | 液氯汽化要吸收一定的能量 |
分析 共价键存在于非金属单质、共价化合物以及部分离子化合物中,分子间作用力只存在与分子晶体,一般为非金属单质以及共价化合物的分子之间,以此解答.
解答 解:A.碘升华克服分子间作用力,共价键没有破坏,故A错误;
B.HI分解生成氢气和碘,共价键破坏,但不能说明有分子间作用力的存在,故B正确;
C.食盐为离子化合物,熔化克服离子键,故C错误;
D.液氯汽化克服分子间作用力,共价键没有破坏,故D错误.
故选B.
点评 本题考查化学键和晶体类型,为高频考点,注意把握共价键以及分子间作用力的区别,含共价键的化合物不一定为分子晶体,只有分子晶体中存在分子间作用力,题目难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
15.标况下,H2O的质量为xg,含有y个氢原子,则阿伏加德罗常数为( )
| A. | 18y/x | B. | 9y/x | C. | 18y/x mol-1 | D. | 9y/x mol-1 |
16.下列离子方程式的书写正确的是( )
| A. | 实验室用浓盐酸与MnO2反应制Cl2:MnO2+4HCl(浓)$\frac{\underline{\;△\;}}{\;}$Cl2↑+Mn2++2Cl-+2H2O | |
| B. | 向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至Ba2+刚好沉淀完全:Ba2++2OH-+H++${SO}_{4}^{2-}$+${NH}_{4}^{+}$═BaSO4↓+NH3•H2O+H2O | |
| C. | 向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:Ca2++${HCO}_{3}^{-}$+OH-═CaCO3↓+H2O | |
| D. | 将标准状况下112mL氯气通入10mL、1 mol/L的溴化亚铁溶液中:2Br-+Cl2═2Cl-+Br2 |
17.下列电离方程式正确的是( )
| A. | 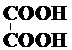 ? ? | B. | Ba(OH)2?Ba2++2OH- | ||
| C. | HCO3-+H2O?H3O++CO32- | D. | NaHCO3═Na++H++CO32- |
14.把0.05mol NaOH固体分别加入到下列100mL液体中,溶液导电性变化较大的是( )
| A. | 0.5mol/L盐酸 | B. | 自来水 | ||
| C. | 0.5mol/L硫酸 | D. | 0.5mol/L 氢氧化钡 |

 ,该反应的类型是取代反应.
,该反应的类型是取代反应.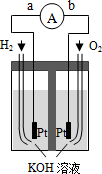 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图.该电池电池表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图.该电池电池表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答: