题目内容
16.下列离子方程式的书写正确的是( )| A. | 实验室用浓盐酸与MnO2反应制Cl2:MnO2+4HCl(浓)$\frac{\underline{\;△\;}}{\;}$Cl2↑+Mn2++2Cl-+2H2O | |
| B. | 向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至Ba2+刚好沉淀完全:Ba2++2OH-+H++${SO}_{4}^{2-}$+${NH}_{4}^{+}$═BaSO4↓+NH3•H2O+H2O | |
| C. | 向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:Ca2++${HCO}_{3}^{-}$+OH-═CaCO3↓+H2O | |
| D. | 将标准状况下112mL氯气通入10mL、1 mol/L的溴化亚铁溶液中:2Br-+Cl2═2Cl-+Br2 |
分析 A.盐酸完全电离;
B.Ba2+刚好沉淀完全,生成硫酸钡、水、一水合氨;
C.少量Ca(HCO3)2溶液完全反应,生成碳酸钙、碳酸钠、水;
D.n(Cl2)=$\frac{0.112L}{22.4L/mol}$=0.005mol,n(FeBr2)=0.01mol,由电子可知,只有亚铁离子被氧化.
解答 解:A.用浓盐酸与MnO2反应制Cl2的离子反应为MnO2+2Cl-+4H+$\frac{\underline{\;△\;}}{\;}$Cl2↑+Mn2++2H2O,故A错误;
B.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至Ba2+刚好沉淀完全的离子反应为Ba2++2OH-+H++SO42-+NH4+═BaSO4↓+NH3•H2O+H2O,故B正确;
C.向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液的离子反应为:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-++2H2O,故C错误;
D.n(Cl2)=$\frac{0.112L}{22.4L/mol}$=0.005mol,n(FeBr2)=0.01mol,由电子可知,只有亚铁离子被氧化,发生的离子反应为2Fe2++Cl2═2Cl-+2Fe3+,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、复分解反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
4.下列说法正确的是( )
| A. | 某物质经测定,只含有一种组成元素,则该物质一定是单质 | |
| B. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 | |
| C. | 碱性氧化物均是金属氧化物,酸性氧化物均是非金属氧化物 | |
| D. | 纯净的硫酸是纯净物,而纯净的盐酸是混合物 |
11.关于原电池的叙述中,错误的是( )
| A. | 构成原电池正极和负极的不一定是两种不同的金属 | |
| B. | 原电池是将化学能转化为电能的装置 | |
| C. | 在原电池中,电子流出的一极是负极,发生氧化反应 | |
| D. | 原电池放电时,电流的方向是从负极到正极 |
8.设NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 71gCl2中含有NA个Cl2分子 | |
| B. | 常温常压下,14g氮气中含有2NA个氮原子 | |
| C. | 0.5mol•L-1CaCl2溶液中含有0.5NA个Ca2+ | |
| D. | 标准状况下,33.6L水中含有1.5NA个水分子 |
5.下列过程中,共价键被破坏,不能说明有分子间作用力的存在的是( )
| A. | 碘升华 | B. | HI气体受热分解 | ||
| C. | 食盐熔化 | D. | 液氯汽化要吸收一定的能量 |
6.(Ⅰ)室温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如表所示:
(1)从甲组情况分析,如何判断HA是强酸还是弱酸?a=7时,HA是强酸;a>7时,HA是弱酸
(2)乙组混合溶液中c(A-)和c(Na+)的大小关系是C
A.前者大 B.后者大
C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+)
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):
c(Na+)-c(A-)=10-4-10-10mol/L.
(Ⅱ)某二元酸(化学式用H2B表示)在水中的电离方程式是:
H2B═H++HB- HB-?H++B2-
回答下列问题:
(5)在0.1mol/L的Na2B溶液中,下列粒子浓度关系式正确的是AC.
A.c(B2-)+c(HB-)=0.1mol/L
B.c(B2-)+c(HB-)+c(H2B)=0.1mol/L
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
( III)已知:25℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=1×10-9.
(6)医学上进行消化系统的X射线透视时,常使用BaSO4作内服造影剂.胃酸酸性很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是(用溶解平衡原理解释)对于平衡BaSO4(s)?Ba2+(aq)+SO42-(aq),H+不能减少Ba2+或SO42-的浓度,平衡不能向溶解方向移动.
万一误服了少量BaCO3,应尽快用大量0.5mol/L Na2SO4溶液给患者洗胃,如果忽略洗胃过程中Na2SO4溶液浓度的变化,残留在胃液中的Ba2+浓度仅为2×10-10mol/L.
| 实验 编号 | HA的物质的量 浓度(mol/L) | NaOH的物质的 量浓度(mol/L) | 混合后 溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
(2)乙组混合溶液中c(A-)和c(Na+)的大小关系是C
A.前者大 B.后者大
C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+)
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):
c(Na+)-c(A-)=10-4-10-10mol/L.
(Ⅱ)某二元酸(化学式用H2B表示)在水中的电离方程式是:
H2B═H++HB- HB-?H++B2-
回答下列问题:
(5)在0.1mol/L的Na2B溶液中,下列粒子浓度关系式正确的是AC.
A.c(B2-)+c(HB-)=0.1mol/L
B.c(B2-)+c(HB-)+c(H2B)=0.1mol/L
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
( III)已知:25℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=1×10-9.
(6)医学上进行消化系统的X射线透视时,常使用BaSO4作内服造影剂.胃酸酸性很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是(用溶解平衡原理解释)对于平衡BaSO4(s)?Ba2+(aq)+SO42-(aq),H+不能减少Ba2+或SO42-的浓度,平衡不能向溶解方向移动.
万一误服了少量BaCO3,应尽快用大量0.5mol/L Na2SO4溶液给患者洗胃,如果忽略洗胃过程中Na2SO4溶液浓度的变化,残留在胃液中的Ba2+浓度仅为2×10-10mol/L.
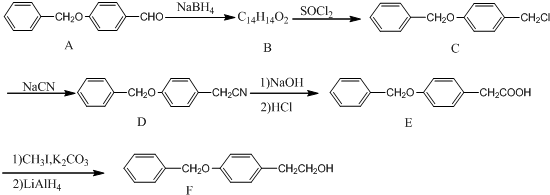
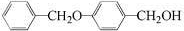 ;由A→B的反应类型是:还原反应.
;由A→B的反应类型是:还原反应.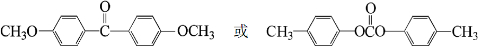 .
. 为原料制备化合物X(
为原料制备化合物X(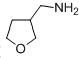 )(结构简式见图)的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:
)(结构简式见图)的合成路线流程图(无机试剂可任选).合成路线流程图示例如下: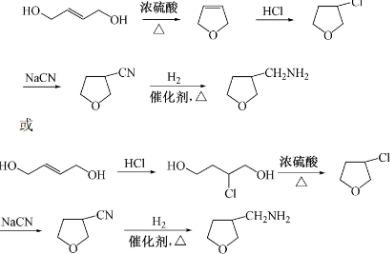 .
. .
.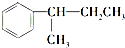 $\stackrel{酸性KMnO_{4}溶液}{→}$
$\stackrel{酸性KMnO_{4}溶液}{→}$ .
.