题目内容
12.利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列叙述正确的是( )| A. | 电解时可以精铜为阳极,以CuSO4溶液为电解液 | |
| B. | 电解时阴极发生还原反应 | |
| C. | 粗铜连接电源负极,其电极反应是Cu-2e-=Cu2+ | |
| D. | 电解结束后,电解质溶液的浓度保持不变 |
分析 A.电解精炼粗铜时,粗铜作阳极、纯铜作阴极,电解质溶液为可溶性的铜盐溶液;
B.电解时,阴极上得电子发生还原反应,阳极上失电子发生氧化反应;
C.粗铜作阳极,阳极连接原电池正极;
D.阳极上Cu、Fe、Zn失电子发生氧化反应,阴极上只有铜离子得电子发生还原反应.
解答 解:A.电解精炼粗铜时,粗铜作阳极、纯铜作阴极,电解质溶液为可溶性的铜盐溶液,阳极金属失电子发生氧化反应,故A错误;
B.电解时,阴极上得电子发生还原反应,阳极上失电子发生氧化反应,阳极反应式为Cu-2e-=Cu2+,故B正确;
C.粗铜作阳极,阳极连接原电池正极,阳极反应式为Cu-2e-=Cu2+,阴极连接原电池负极,故C错误;
D.阳极上Cu、Fe、Zn失电子发生氧化反应,阴极上只有铜离子得电子发生还原反应,溶解的铜小于析出的铜,所以电解后电解质溶液浓度降低,故D错误;
故选B.
点评 本题考查电解原理,为高频考点,明确电解精炼粗铜时阴阳极及电解质成分、各个电极发生的反应即可解答,Ag、Pt会以单质形式进入溶液而转化为阳极泥,题目难度不大.

练习册系列答案
相关题目
2.某高分子化合物含有如下结构片段,对此结构的分析正确的是( )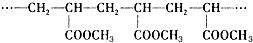
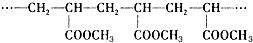
| A. | 它是缩聚反应的产物 | B. | 高分子的分子式是C4H6O2 | ||
| C. | 合成它的单体是CH2=CHCOOCH3 | D. | 高分子的相对分子质量是86 |
3.将一定量A、B装入容积为1L的恒温密闭容器中,发生反应:2A(g)+bB(g)?cC(g),1min时达到平衡,C的浓度为x mol•L-1.若保持温度不变,将密闭容器的容积压缩为原来的$\frac{1}{2}$,重新达到平衡后,C的浓度为2.5x mol•L-1,下列说法正确的是( )
| A. | 化学计量数的关系:b<c | |
| B. | 容器的容积减小后,该反应的逆反应速率减小 | |
| C. | 原容器中用B浓度变化表示该反应在1 min内的速率为$\frac{cx}{b}$mol•(L•min)-1 | |
| D. | 若保持温度和容器容积不变,充入氦气(不参与反应),平衡不发生移动 |
20.某酯A的化学式为C6H12O2,已知A~E有如图转化关系,C、E均不能发生银镜反应,则A结构可能有( )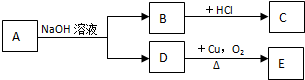

| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
4.下列有关水的认识,你认为正确的是( )
| A. | 用自来水烧开水热水壶底常沉积一层水垢,说明蒸馏水不是纯净物 | |
| B. | 用自来水配制的硝酸银溶液出现浑浊现象,说明自来水中含有氯化银杂质 | |
| C. | 用蒸馏的方法可以从海水中提取淡水,说明水和食盐的沸点不同 | |
| D. | 少量水洒到烧旺的煤炉中火焰会更猛烈,说明一定条件下水能燃烧 |
1.为了使埋在地下的钢管不易生锈,设计了如下几种方案,将钢管:①用导线与铅板连接 ②用导线与锌板连接 ③用导线与碳棒连接 ④与直流电源负极连接 ⑤直流电源正极连接,其中可采取的方法是( )
| A. | ①④ | B. | ②④ | C. | ②③ | D. | ①⑤ |
3.下列说法正确的是 ( )
| A. | CH3Cl、CH2Cl2.CHCl3.CCl4互为同系物 | |
| B. | O2和O3互为同素异形体 | |
| C. | 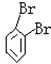 和 和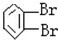 互为同分异构体 互为同分异构体 | |
| D. | 1H、2H、3H互为同位素 |