题目内容
【题目】通常状况下,![]() 、
、![]() 和
和![]() 是三种气态单质。
是三种气态单质。![]() 的组成元素是第3周期原子半径最小的元素(稀有气体元素除外);
的组成元素是第3周期原子半径最小的元素(稀有气体元素除外);![]() 和
和![]() 均由元素
均由元素![]() 组成,
组成,![]() 能氧化
能氧化![]() ,反应的离子方程式为
,反应的离子方程式为 。
。
(1)写出物质的分子式:![]() ______,
______,![]() ______,
______,![]() ______。
______。
(2)![]() 与
与![]() 的关系是______(填序号)。
的关系是______(填序号)。
a.互为同位素 b.属于同一物质
c.互为同素异形体 d.互为同分异构体
(3)导致大气中![]() 减少的主要物质是______。
减少的主要物质是______。
(4)将![]() 和二氧化硫分别通入品红溶液中,都能使品红溶液褪色。利用褪色的溶液区别二者的实验方法是________________________。
和二氧化硫分别通入品红溶液中,都能使品红溶液褪色。利用褪色的溶液区别二者的实验方法是________________________。
(5)举例说明![]() 的氧化性比硫单质的氧化性强:________________________(用化学方程式表示)。
的氧化性比硫单质的氧化性强:________________________(用化学方程式表示)。
【答案】![]()
![]()
![]() c 氟氯烃(或氟利昂) 加热褪色后的溶液,若溶液恢复红色,则通入的气体为
c 氟氯烃(或氟利昂) 加热褪色后的溶液,若溶液恢复红色,则通入的气体为![]() ;若溶液不变红,则通入的气体是
;若溶液不变红,则通入的气体是![]()
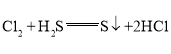 (其他合理答案也可)
(其他合理答案也可)
【解析】
通常状况下,X、Y和Z是三种气态单质,X的组成元素是第三周期原子半径最小的元素(稀有气体元素除外),则X为Cl2;Y和Z均由元素R组成,反应Y+2I-+2H+═I2+Z+H2O常作为Y的鉴定反应,由元素守恒可知,Y、Z为O元素的同素异形体,R为O元素;可推知Y为O3、Z为O2;据此分析解答。
(1)根据上述分析,X、Y和Z的分子式分别为Cl2、O3、O2,故答案为:Cl2;O3;O2;
(2)Y为O3、Z为O2,都是由氧元素形成的结构不同的单质,二者互为同素异形体,故答案为:c;
(3)氟利昂能够破坏臭氧层,导致大气中![]() 减少,故答案为:氟氯烃(或氟利昂);
减少,故答案为:氟氯烃(或氟利昂);
(4)将O3和二氧化硫分别通入品红溶液,都能使品红褪色,由于臭氧具有强氧化性,褪色后的溶液不能恢复原来的颜色,二氧化硫是与有色物质结合生成无色不稳定的物质,加热后恢复原来的颜色,因此用褪色的溶液区别O3和二氧化硫的实验方法为:加热褪色后的溶液,若溶液恢复红色,则原通入气体为SO2;若溶液不变红,则原通入气体是O3,故答案为:加热褪色后的溶液,若溶液恢复红色,则原通入气体为SO2;若溶液不变红,则原通入气体是O3;
(5)氯气的氧化性比硫单质的氧化性强,能够将硫从硫化氢(或氢硫酸)中置换出来,反应的化学方程式为:H2S+Cl2═S+2HCl,故答案为:H2S+Cl2═S+2HCl。

【题目】苯甲酸乙酯可由苯甲酸与乙醇在浓硫酸共热下反应制得,反应装置如图(部分装置省略),反应原理如下:
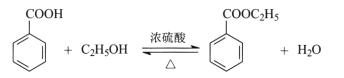
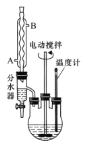
实验操作步骤:
①向三颈烧瓶内加入12.2g苯甲酸、25mL乙醇、20mL苯及4mL浓硫酸,摇匀,加入沸石。
②装上分水器、电动搅拌器和温度计,加热至分水器下层液体接近支管时将下层液体放入量筒中。继续蒸馏,蒸出过量的乙醇,至瓶内有白烟(约3h),停止加热。
③将反应液倒入盛有80mL冷水的烧杯中,在搅拌下分批加入碳酸钠粉末至溶液无二氧化碳逸出,用pH试纸检验至呈中性。
④用分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层。用无水CaC12干燥,粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接收210-213℃的馏分,最终通过蒸馏得到纯净苯甲酸乙酯12.8mL。
可能用到的有关数据如下:
相对分子质量 | 密度(g/cm3) | 沸点/℃ | 溶解性 | |
苯甲酸 | 122 | 1.27 | 249 | 微溶于水,易溶于乙醇、乙醚 |
苯甲酸乙酯 | 150 | 1.05 | 211-213 | 微溶于热水,溶于乙醇、乙醚 |
乙醇 | 46 | 0.79 | 78.5 | 易溶于水 |
乙醚 | 74 | 0.73 | 34.5 | 微溶于水 |
回答以下问题:
(1)反应装置中分水器上方的仪器名称是______,其作用是____
(2)步骤①中加浓硫酸的作用是_________,加沸石的目的是______。
(3)步骤②中使用分水器除水的目的是_________。
(4)步骤③中加入碳酸钠的目的是________ 。
(5)步骤④中有机层从分液漏斗的____(选填“上口倒出”或“下口放出”)。
(6)本实验所得到的苯甲酸乙酯产率是________%。
【题目】现有几组物质的熔点数据如表所示。
A组 | B组 | C组 | D组 |
金刚石:3550℃ |
|
|
|
硅晶体:1410℃ |
|
|
|
硼晶体:2300℃ |
|
|
|
二氧化硅:1723℃ |
|
|
|
请回答下列问题:
(1)A组属于______晶体,其熔化时克服的微粒间的作用力是______。
(2)B组晶体共同的物理性质是______(填序号)。
A.有金属光泽 B.有导电性 C.有导热性 D.有延展性
(3)C组中酸性最弱的是______,最不稳定的是______。
(4)D组晶体可能具有的性质是______(填序号)。
A.硬度小 B.水溶液能导电 C.固体能导电 D.熔融状态下能导电