题目内容
(1)要除去氯化钠里混有的少量溴化钠和碘,可先将固体混合物 ,使碘 ,把碘除去;再将处理过的残渣溶于水,向溶液中先 ,充分反应后,再加入适量的 ,分层后进行 操作,最后将溶液蒸发结晶,即得纯净的NaCl.
(2)盛放溴水的试剂瓶不能用橡胶塞,其原因是 ;装碘的瓶子不能用铁盖,其原因是 ;不能用自来水配制碘化钾溶液,其原因是 .
(2)盛放溴水的试剂瓶不能用橡胶塞,其原因是
考点:氯、溴、碘及其化合物的综合应用,物质分离和提纯的方法和基本操作综合应用
专题:卤族元素
分析:(1)氯气和与溴化钠反应生成氯化钠和溴,溴易挥发,碘易升华,从溶液中得到氯化钠晶体,可用蒸发、结晶的方法;
(2)溴可腐蚀橡胶,碘易升华,可与铁反应,自来水中含有氯气分子,可与碘化钾反应.
(2)溴可腐蚀橡胶,碘易升华,可与铁反应,自来水中含有氯气分子,可与碘化钾反应.
解答:
解:(1)要除去氯化钠里混有的少量溴化钠和碘,可先将固体混合物,可先将混合物加热,使碘升华,再将处理过的残渣溶于水,向溶液中先通入适量的氯气,氯气置换出溴,加入适量的有机溶剂,然后分液,最后将溶液蒸发结晶,即得纯净的NaCl,
故答案为:加热;升华;通入适量的氯气;有机溶剂;分液;
(2)盛放溴水的试剂瓶不能用橡胶塞,其原因是溴蒸气会腐蚀橡胶,碘易升华,可与铁反应而腐蚀铁,自来水中含有氯气分子,可与碘化钾反应,
故答案为:溴蒸气会腐蚀橡胶;碘易升华,碘蒸气与铁盖接触,易发生反应,使铁发生腐蚀;自来水中含有的少量的氯分子等能跟KI反应.
故答案为:加热;升华;通入适量的氯气;有机溶剂;分液;
(2)盛放溴水的试剂瓶不能用橡胶塞,其原因是溴蒸气会腐蚀橡胶,碘易升华,可与铁反应而腐蚀铁,自来水中含有氯气分子,可与碘化钾反应,
故答案为:溴蒸气会腐蚀橡胶;碘易升华,碘蒸气与铁盖接触,易发生反应,使铁发生腐蚀;自来水中含有的少量的氯分子等能跟KI反应.
点评:本题综合考查氯气以及混合物的性质,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,有利于培养学生的良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
相关题目
有关Na2CO3和NaHCO3的性质,下列叙述错误的是( )
| A、等质量的Na2CO3和NaHCO3与足量的盐酸反应,在相同条件下NaHCO3产生的CO2气体体积大 |
| B、同一温度下,与等浓度的盐酸反应时,NaHCO3比Na2CO3剧烈 |
| C、与同种酸反应生成等量的CO2时,所消耗的酸的量相等 |
| D、将石灰水加入到NaHCO3溶液中将会产生沉淀 |
欲从苯酚的乙醇溶液中分离苯酚和乙醇,有下列操作:
①过滤 ②蒸馏 ③静置分液 ④加入足量的金属钠 ⑤加入足量的NaOH溶液 ⑥通入过量的二氧化碳 ⑦加入足量的FeCl3溶液 ⑧加入乙酸与浓硫酸混合液加热.
合理的实验操作步骤及顺序是( )
①过滤 ②蒸馏 ③静置分液 ④加入足量的金属钠 ⑤加入足量的NaOH溶液 ⑥通入过量的二氧化碳 ⑦加入足量的FeCl3溶液 ⑧加入乙酸与浓硫酸混合液加热.
合理的实验操作步骤及顺序是( )
| A、④⑤③ | B、⑥①⑤③ |
| C、⑧①⑦③ | D、⑤②⑥③ |
短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4,下列说法正确的是( )
| A、W、Y、Z的非金属性大小顺序一定是Z>Y>W |
| B、W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z |
| C、Y、Z形成的分子空间构型可能是正四面体 |
| D、XZ3中含有离子键 |
下列说法正确的是( )
| A、键能越大,表示该分子越容易受热分解 |
| B、共价键都具有方向性 |
| C、在分子中,两个成键的原子间的距离叫键长 |
| D、H-Cl的键能为431.8kJ?mol-1,H-Br的键能为366kJ?mol-1,说明HCl比HBr分子稳定 |
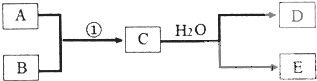 已知物质A、B、C、D、E是由短周期元素构成的单质或化合物,它们可发生如图所示的转化关系:
已知物质A、B、C、D、E是由短周期元素构成的单质或化合物,它们可发生如图所示的转化关系: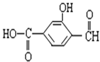 具有复合官能团的复杂有机物:官能团具有各自的独立性,在不同条件下所发生的化学性质可分别从各官能团讨论.如:具有三个官能团:
具有复合官能团的复杂有机物:官能团具有各自的独立性,在不同条件下所发生的化学性质可分别从各官能团讨论.如:具有三个官能团: