题目内容
短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4,下列说法正确的是( )
| A、W、Y、Z的非金属性大小顺序一定是Z>Y>W |
| B、W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z |
| C、Y、Z形成的分子空间构型可能是正四面体 |
| D、XZ3中含有离子键 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:W、X原子的最外层电子数之比为4:3,因为主族元素,则最外层电子数分别为4、3,分别为ⅣA、ⅢA族元素,而短周期主族元素W、X、Y、Z的原子序数依次增大,可知W为C元素,X为Al元素,Z原子比X原子的核外电子数多4,应为Cl元素,Y为原子序数介于14~16之间的元素,以此解答该题.
解答:
解:W、X原子的最外层电子数之比为4:3,因为主族元素,则最外层电子数分别为4、3,分别为ⅣA、ⅢA族元素,而短周期主族元素W、X、Y、Z的原子序数依次增大,可知W为C元素,X为Al元素,Z原子比X原子的核外电子数多4,应为Cl元素,Y为原子序数介于14~16之间的元素,
A.如Y为Si元素,则非金属性小于C,故A错误;
B.由以上分子可知W在第二周期,而X、Y、Z在第三周期,则W的原子半径最小,故B错误;
C.如Y为Si,则Y、Z形成的分子为SiCl4,空间构型是正四面体,故C正确;
D.AlCl3为共价化合物,含有共价键,故D错误.
故选C.
A.如Y为Si元素,则非金属性小于C,故A错误;
B.由以上分子可知W在第二周期,而X、Y、Z在第三周期,则W的原子半径最小,故B错误;
C.如Y为Si,则Y、Z形成的分子为SiCl4,空间构型是正四面体,故C正确;
D.AlCl3为共价化合物,含有共价键,故D错误.
故选C.
点评:本题考查结构与位置关系、元素周期律、微粒半径比较等,难度中等,推断元素是关键,注意核外电子排布规律.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
下列说法正确的是( )
| A、HCHO溶液、(NH4)2SO4溶液均能使蛋白质变性 |
| B、煤的干馏是物理变化,煤的气化和液化是化学变化 |
| C、纤维素、蛋白质、油脂均为天然高分子化合物 |
D、聚碳酸酯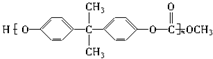 中含有 中含有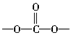 结构 结构 |
下列排序正确的是( )
| A、酸性:碳酸<苯酚<醋酸 |
| B、碱性:Ca(OH)2<Mg(OH)2<KOH |
| C、密度:溴苯<苯<水 |
| D、沸点:PH3<NH3<H2O |
有关氧化还原反应的叙述正确的是( )
| A、物质所含元素化合价升高的反应是还原反应 |
| B、氧化还原反应的实质是有氧元素的得失 |
| C、氧化还原反应的实质是元素化合价的升降 |
| D、有单质参加或生成的化学反应不一定是氧化还原反应 |
下列物质的性质比较,不正确的是( )
| A、酸性:H2SO4>HClO4>HBrO4 |
| B、碱性:RbOH>KOH>NaOH |
| C、非金属性:Cl>S>P |
| D、气态氢化物稳定性:HF>HCl>HBr |
C8H16的烯烃各同分异构体中,其中与HBr发生加成反应只生成一种产物的有( )
| A、2种 | B、3种 | C、4种 | D、5种 |
在含有NaBr和KI的溶液里通入足量的氯气,然后将溶液蒸干并灼烧,最后留下的固体物质是( )
| A、KCl和I2 |
| B、NaCl和Br2 |
| C、NaCl、KCl和I2 |
| D、NaCl和KCl |