题目内容
.某化学兴趣小组测定某FeCl3样品(只含少量FeCl2杂质)中铁元素的质量分数,按以下实验步骤进行操作:
① 称取a g样品,置于烧杯中;
② 加入适量盐酸和蒸馏水,使样品溶解,然后准确配制成250.00mL溶液;
③量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;
④ 加入过量氨水,充分搅拌,使沉淀完全;
⑤ 过滤,洗涤沉淀;
⑥ 将沉淀转移到某容器内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;
⑦……。
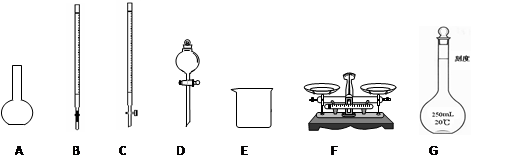
请根据上面叙述,回答:
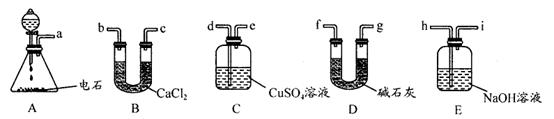
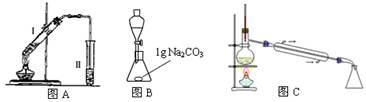
(1)上图所示仪器中,本实验步骤①②③中必须用到的仪器是E和 (填字母)。
(2)写出步骤④中发生反应的离子方程式 。
(3)样品中的杂质Fe2+有较强的还原性,完成并配平下列反应的离子方程式
Fe2+ + ClO3— + = Fe3+ + Cl— + H2O
从理论上分析,上述实验中若将氯水改为NaClO3时,对实验结果造成 (填偏大、偏小或不影响),
(4)若容器质量是W1 g,最终容器和固体的总质量是W2 g,则样品中铁元素的质量分数为 。(列出算式,不需化简)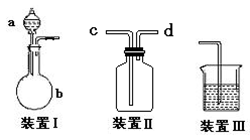
① 称取a g样品,置于烧杯中;
② 加入适量盐酸和蒸馏水,使样品溶解,然后准确配制成250.00mL溶液;
③量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;
④ 加入过量氨水,充分搅拌,使沉淀完全;
⑤ 过滤,洗涤沉淀;
⑥ 将沉淀转移到某容器内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;
⑦……。

请根据上面叙述,回答:
(1)上图所示仪器中,本实验步骤①②③中必须用到的仪器是E和 (填字母)。
(2)写出步骤④中发生反应的离子方程式 。
(3)样品中的杂质Fe2+有较强的还原性,完成并配平下列反应的离子方程式
Fe2+ + ClO3— + = Fe3+ + Cl— + H2O
从理论上分析,上述实验中若将氯水改为NaClO3时,对实验结果造成 (填偏大、偏小或不影响),
(4)若容器质量是W1 g,最终容器和固体的总质量是W2 g,则样品中铁元素的质量分数为 。(列出算式,不需化简)

(1)C F G
(2)Fe3+ +3NH3H2O=Fe(OH)3↓+ 3 NH4+
(3)6Fe2+ + ClO3— + 6 H+= 6Fe3+ + Cl— + 3H2O ,无影响,

(2)Fe3+ +3NH3H2O=Fe(OH)3↓+ 3 NH4+
(3)6Fe2+ + ClO3— + 6 H+= 6Fe3+ + Cl— + 3H2O ,无影响,

(1)实验步骤①是称量需要用到天平F,步骤②溶解并配制溶液需要用到容量瓶G,步骤③是取一定量的溶液,由于该溶液呈酸性且Fe3+具有氧化性所以要用酸式滴定管C。
(2)步骤④是向的溶液中Fe3+加入碱性的氨水,Fe3+会与碱反应生成Fe(OH)3,反应的离子反应方程式为Fe3+ +3NH3H2O=Fe(OH)3 ↓+ 3 NH4+
(3)根据氧化还原反应中得失电子守恒,先配平电子,然后根据电荷守恒确定空格中为氢离子,并配平,结果为6Fe2+ + ClO3— + 6 H+= 6Fe3+ + Cl— + 3H2O;由于最后称量的是Fe2O3这一步只是将Fe2+氧化为Fe3+,只要能够实现该转化并且不对后面的沉淀产生影响都是可以的,所以若将氯水改为NaClO3时,对实验结果无影响。
(4)容器中剩余的固体为Fe2O3,并且Fe2O3的质量为(W2- W1)g,根据铁元素的质量分数计算铁元素的质量为 g,又这些铁元素只是25.00mL溶液中的铁元素质量,则250mL溶液中铁元素可以计算出来,在除以样品总质量即为铁元素的质量分数,为:
g,又这些铁元素只是25.00mL溶液中的铁元素质量,则250mL溶液中铁元素可以计算出来,在除以样品总质量即为铁元素的质量分数,为:
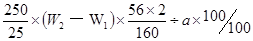
(2)步骤④是向的溶液中Fe3+加入碱性的氨水,Fe3+会与碱反应生成Fe(OH)3,反应的离子反应方程式为Fe3+ +3NH3H2O=Fe(OH)3 ↓+ 3 NH4+
(3)根据氧化还原反应中得失电子守恒,先配平电子,然后根据电荷守恒确定空格中为氢离子,并配平,结果为6Fe2+ + ClO3— + 6 H+= 6Fe3+ + Cl— + 3H2O;由于最后称量的是Fe2O3这一步只是将Fe2+氧化为Fe3+,只要能够实现该转化并且不对后面的沉淀产生影响都是可以的,所以若将氯水改为NaClO3时,对实验结果无影响。
(4)容器中剩余的固体为Fe2O3,并且Fe2O3的质量为(W2- W1)g,根据铁元素的质量分数计算铁元素的质量为
 g,又这些铁元素只是25.00mL溶液中的铁元素质量,则250mL溶液中铁元素可以计算出来,在除以样品总质量即为铁元素的质量分数,为:
g,又这些铁元素只是25.00mL溶液中的铁元素质量,则250mL溶液中铁元素可以计算出来,在除以样品总质量即为铁元素的质量分数,为: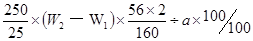

练习册系列答案
相关题目