题目内容
6.下列说法中正确的是( )| A. | 实验室制乙炔时用启普发生器得到的气体再用硫酸铜溶液除杂即可得到纯净的乙炔 | |
| B. | 实验室制得的乙炔气体直接通入酸性高锰酸钾溶液后,若紫色褪去则能证明乙炔中含有不饱和键可以被氧化剂氧化 | |
| C. | 芳香烃即可从石油的催化重整得到,也可从煤中直接分离得到 | |
| D. | 通过石油分馏得到的脂肪烃依然是混合物 |
分析 A.实验室不能用启普发生器制取乙炔气体;
B.生成的乙炔中含有硫化氢等还原性气体;
C.石油的催化重整能得到小分子的烷烃及烯烃;
D.石油分馏得到的脂肪烃是多种烃的混合物.
解答 解:A.此反应大量放热,生成的氢氧化钙是糊状物,反应很剧烈,应选用分液漏斗,以便控制水的流速,故实验室不能用启普发生器制取乙炔气体,应用分液漏斗和平底烧瓶,故A错误;
B.生成的乙炔中含有硫化氢等还原性气体,硫化氢也能使酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,故B错误;
C.石油的催化重整能得到小分子的烷烃及烯烃,不能得到芳香烃,故C错误;
D.分馏石油得到的各个馏分为烃类物质的混合物,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及仪器选取、物质检验、石油分馏及催化重整等知识点,明确实验原理及仪器作用是解本题关键,易错选项是B.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
10.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 1molFeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 0.2mol S在空气中充分燃烧,转移电子数为0.6NA | |
| C. | 0.1molCl2与足量的水充分反应,转移电子数为0.1NA | |
| D. | 1.5molNa2O2与足量的二氧化碳充分反应,转移电子数为1.5NA |
1.短周期元素A、B、C、D的原子序数依次递增,A与C同主族,B与D同主族,A、C原子的最外层电子数之和等于B原子的次外层电子数,D元素原子最外层电子数为电子层数的2倍,四种元素原子的核电荷数之和为36.则下列叙述正确的是( )
| A. | C元素的单质在B元素的单质中燃烧,产物1mol与足量的水反应转移电子数为NA | |
| B. | 由上述元素形成的化合物只有一种具有漂白性 | |
| C. | B、C、D三种元素形成的化合物的水溶液用惰性电极电解时,溶液pH一定不变 | |
| D. | A、B形成化合物的沸点高于A、C形成化合物的沸点,因为前者分子间形成了氢键 |
11.引起下列环境污染的原因不正确的是( )
| A. | 重金属、农药和难分解有饥物等会造成水体污染 | |
| B. | 装饰材料中的甲醛、芳香烃及氡等会造成居室污染 | |
| C. | SO2、NO2或CO2都会导致酸雨的形成 | |
| D. | CO2和氟氯烃等物质的大量排放会造成温室效应的加剧 |
18.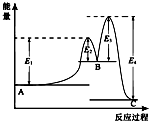 某反应由两步反应A?B?C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
某反应由两步反应A?B?C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
 某反应由两步反应A?B?C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
某反应由两步反应A?B?C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )| A. | 两步反应均为吸热反应 | B. | 整个反应中△H=E1+E3-E2-E4 | ||
| C. | 加入催化剂会改变反应的焓变 | D. | 三种化合物中B最稳定 |
15.下列微粒可以大量共存于同一溶液中的是( )
| A. | NH4+、CH3COO-、Ca2+、Cl- | B. | Ca2+、Ag+、SO42-、NO3- | ||
| C. | Cu2+、H+、S2-、NO3- | D. | C6H5O-、Fe3+、H+、Cl- |
16.化学与生活、生产息息相关,下列说法中错误的是( )
| A. | 海鲜中有较多Zn元素,经常食用可提高免疫力 | |
| B. | 聚乳酸可用作手术缝合纱线、缓释药物材料 | |
| C. | 氨冷冻系统可用于禽类加工厂的冷库 | |
| D. | 用浓硫酸处理碱性工业废水 |
 海洋是巨大的资源宝库,具有美好的前景.
海洋是巨大的资源宝库,具有美好的前景. 所示.
所示.