题目内容
14.图1中X为中学化学中的一种常见的盐,H为单质,F为淡黄色固体,M为常见的金属,图中部分反应产物及反应条件已略去.
(1)F的电子式为
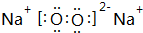 ;G的化学式为Fe(OH)3.
;G的化学式为Fe(OH)3.(2)反应①的离子方程式为3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O.
(3)若向100mL 盐X的溶液中加入9g金属单质M的粉末,充分搅拌后,过滤,烘干得(9.32g固体C,则滤液A中溶质的物质的量浓度为0.4mol/L(假设溶液体积不变).
(4)盐酸可通过氯碱工业制取,氯碱工业是用电解饱和NaCl溶液的方法来制取NaOH、Cl2和H2,并以它们为原料生产一系列化工产品的工业生产.某化学兴趣小组进行有关电解食盐水的探究实验,电解装置如图2所示.
实验一:电解饱和食盐水.
实验二:电解不饱和食盐水及产物分析.
相同条件下,电解1mol/L NaCl溶液并收集两极产生的气体.在X处收集到V1mL气体,同时在Y处收集到V2mL
气体,停止电解.结果发现V2<V1,且与电解饱和食盐水相比,Y处收集到的气体颜色明显较浅.经讨论分析,导致上述现象的原因有:
ⅰ.有部分C12溶解于NaCl溶液中;
ii.有O2生成.
①设计实验证明有部分C12溶解于NaCl溶液中,实验方案及现象为取少量石墨电极附近溶液,滴在淀粉KI试纸上,试纸变蓝.
②证明有O2生成并测定O2的体积.按如如图3所示装置进行实验.通过注射器缓缓地将在Y处收集到的V2mL气体全部推入装置A(盛有足量试剂)中,最终,量气管中收集到V3mL气体(设V1、V2、V3均在相同条件下测得).装置A的作用是完全吸收氯气.
③实验中是否需要预先除净装置中的空气?否(填“是”或“否”).
④实验二中,在石墨电极上生成Cl2的总体积为(V1-2V3)mL(用代数式表示).
分析 F为淡黄色固体,与盐X反应得到蓝色沉淀Y与气体单质H,则F为Na2O2,Y为Cu(OH)2,H为O2,X含有Cu2+.M是常见金属,与铜盐X发生置换反应,沉淀C中含有Cu及未反应的金属M,滤液A中加入盐酸生成的无色气体D遇空气变为红棕色,故D为NO,X为Cu(NO3)2,由A→D生物反应,可知M为Fe,A为Fe(NO3)2,B为铁盐,G为Fe(OH)3,E为Fe2O3;
(4)①部分C12溶解于NaCl溶液中,溶解的氯气可以氧化碘离子为碘单质,碘遇淀粉变蓝色,据此设计;
②Y为阳极,收集到的V2mL气体中主要是氯气,所以证明有O2生成首先要除去氯气,当量气管的右侧液面上升,则说明含有氧气生成;
③空气对压强不影响,所以实验中不需要预先除净装置中的空气;
④阴极X处收集到的氢气为V1mL,阳极Y处收集到为氯气和氧气,最终量气管中收集到V3mL气体为氧气,设在石墨电极上生成Cl2的总体积为xml,则根据电解阴阳两极的得失电子守恒计算.
解答 解:F为淡黄色固体,与盐X反应得到蓝色沉淀Y与气体单质H,则F为Na2O2,Y为Cu(OH)2,H为O2,X含有Cu2+.M是常见金属,与铜盐X发生置换反应,沉淀C中含有Cu及未反应的金属M,滤液A中加入盐酸生成的无色气体D遇空气变为红棕色,故D为NO,X为Cu(NO3)2,由A→D生物反应,可知M为Fe,A为Fe(NO3)2,B为铁盐,G为Fe(OH)3,E为Fe2O3.
(1)F为Na2O2,电子式为 ;G的化学式为Fe(OH)3,
;G的化学式为Fe(OH)3,
故答案为: ;Fe(OH)3;
;Fe(OH)3;
(2)反应①的离子方程式为:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O,
故答案为:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O;
(3)设Fe2+的物质的量为xmol,则:
Cu2++Fe═Fe2++Cu 质量增重
1mol 64g-56g=8g
xmol 9.32g-9g=0.32g
故1mol:xmol=8g:0.32g,解得x=0.04,则滤液A中溶质的物质的量浓度为$\frac{0.04mol}{0.1L}$=0.4mol/L,
故答案为:0.4mol/L;
(4)①因为氯气可使湿润的淀粉KI试纸变蓝,证明有部分C12溶解于NaCl溶液中,可取少量石墨电极附近溶液,滴在淀粉KI试纸上,试纸变蓝,说明含有氯气,
故答案为:取少量石墨电极附近溶液,滴在淀粉KI试纸上,试纸变蓝;
②Y为阳极,收集到的V2mL气体中主要是氯气,所以证明有O2生成首先要除去氯气,当量气管的右侧液面上升,则说明含有氧气生成,则装置A的作用是完全吸收氯气,故答案为:完全吸收氯气;
故答案为:完全吸收氯气;
③空气对压强不影响,所以实验中不需要预先除净装置中的空气,
故答案为:否;
④阴极X处收集到的氢气为V1mL,阳极Y处收集到为氯气和氧气,最终量气管中收集到V3mL气体为氧气,设在石墨电极上生成Cl2的总体积为xml,则根据电解阴阳两极的得失电子守恒,V1×2=x×2+V3×4,所以x=V1-2V3,故答案为:(V1-2V3).
点评 本题考查无机物推断、探究实验,属于拼合型题目,题目综合性较强,需要学生具备扎实的基础,难度中等.

| A. | CH4(C2H4):酸性高锰酸钾溶液 | |
| B. | NaHCO3溶液(少量Na2CO3):通入足量的CO2气体 | |
| C. | 苯(混有Br2):加NaOH溶液洗涤、静置、分液 | |
| D. | FeCl3溶液(FeCl2):通入适量氯气 |
| A. | 氢氧化铁溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| B. | 盛放烧碱的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O | |
| C. | 向碳酸氢铵溶液中加过量石灰水并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 用酸化的高锰酸钾溶液氧化双氧水:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
| A. | 化学反应中物质变化的实质是旧化学键断裂和新化学键形成 | |
| B. | 燃烧可看成“储存”在物质内部的能量转化为热能、光能等释放出来 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 在化学反应中,破坏旧化学键吸收的能量大于形成新化学键释放的能量时,该反应是放热反应 |
| A. | 乙烯使溴的四氯化碳溶液褪色 | B. | 由乙酸制乙酸乙酯 | ||
| C. | 乙烯使酸性高锰酸钾溶液褪色 | D. | 甲烷与氯气在光照条件下发生反应 |
| A. | pH=0 的溶液中:Mg2+、Fe3+、NO3-、SO42- | |
| B. | 能使pH试纸变红色的溶液中:Na+、AlO2-、S2-、CO32- | |
| C. | 含有大量Fe3+的溶液:SCN-、I-、K+、Br- | |
| D. | 由水电离出的c(OH-)=1×10-13 mol•L-1的溶液中:NH4+、Al3+、NO3-、Cl- |
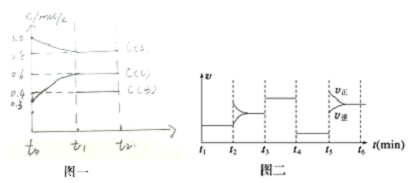
| A. | t4-t5阶段改变的条件为减小压强 | |
| B. | B的起始物质的量为1.0 mol | |
| C. | 在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,要达到t1时刻同样的平衡(与t1时刻浓度相同),a、b、c要满足的条件为a+$\frac{2c}{3}$=2.4和b+$\frac{c}{3}$=1.2 | |
| D. | 此温度下该反应的化学方程式为2A(g)+B(g)?2C(g) |
 cC(g)。反应过程中,物质A的含量(A%)和C的含量(C%)随温度(T)的变化曲线如图所示,下列说法正确的是
cC(g)。反应过程中,物质A的含量(A%)和C的含量(C%)随温度(T)的变化曲线如图所示,下列说法正确的是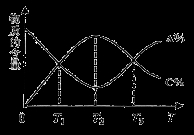
 方向移动
方向移动