题目内容
【题目】2-甲基-1,3-丁二烯是一种重要的化工原料。可以发生以下反应。已知:
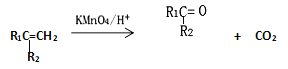
![]()
![]()
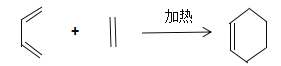

请回答下列问题:
(1)2-甲基-1,3-丁二烯可以与氢气、溴水等发生加成反应。
①完全与氢气加成所得有机产物的名称____________;
②与溴水发生1,2-加成所得有机产物的结构简式为____________ 和 _____________;
③与溴水发生1,4-加成反应的化学方程式为_______________________________________。
(2)B为含有六元环的有机物,写出2-甲基-1,3-丁二烯与乙烯反应的化学方程式________________________________________。
(3)Y(![]() )是天然橡胶的主要成分。能发生的反应有_________(填标号)。
)是天然橡胶的主要成分。能发生的反应有_________(填标号)。
A.加成反应 B.氧化反应 C.酯化反应
(4)X的分子式为C3H4O3,其结构简式为_________________;X与乙醇发生酯化反应的化学方程式______________________________。
【答案】2-甲基丁烷 (或异戊烷) BrCH2CBr (CH3)CH=CH2 CH2=C(CH3)CH BrCH2Br CH2=C(CH3)CH=CH2+Br2→BrCH2C(CH3)=CHCH2Br CH2=C(CH3)CH=CH2+CH2=CH2 → ![]() AB
AB ![]()
![]()
【解析】
(1)2-甲基-1,3-丁二烯可以与氢气完全加成反应生成CH3-CH(CH3)-CH2-CH3,根据系统命名法可知,该物质为2-甲基丁烷;2-甲基-1,3-丁二烯与溴水发生1,2-加成可能生成两种产物,结构简式为:BrCH2CBr(CH3)CH=CH2 ,CH2=C(CH3)CHBrCH2Br;2-甲基-1,3-丁二烯与溴水发生1,4-加成反应时,1,2号碳原子和3,4号碳原子之间的碳碳双键断裂,在2,3号碳原子之间形成一个碳碳双键,即生成BrCH2C(CH3)=CHCH2Br,反应方程式为:CH2=C(CH3)CH=CH2+Br2→BrCH2C(CH3)=CHCH2Br,故答案为:2-甲基丁烷(或异戊烷),BrCH2CBr(CH3)CH=CH2,CH2=C(CH3)CH BrCH2Br,CH2=C(CH3)CH=CH2+Br2→BrCH2C(CH3)=CHCH2Br;
(2)2-甲基-1,3-丁二烯与乙烯反应形成六元环,即在2-甲基-1,3-丁二烯的2,3号碳原子上形成碳碳双键,连接打开双键的乙烯,即生成![]() ,所以化学方程式为:CH2=C(CH3)CH=CH2+CH2=CH2→
,所以化学方程式为:CH2=C(CH3)CH=CH2+CH2=CH2→![]() ,故答案为:CH2=C(CH3)CH=CH2+CH2=CH2 →
,故答案为:CH2=C(CH3)CH=CH2+CH2=CH2 →![]() ;
;
(3)Y(![]() )是天然橡胶的主要成分。根据Y的结构简式可知,Y中含有碳碳双键,所以Y能发生加成反应、氧化反应,故AB正确;故选AB;
)是天然橡胶的主要成分。根据Y的结构简式可知,Y中含有碳碳双键,所以Y能发生加成反应、氧化反应,故AB正确;故选AB;
(4)X的分子式为C3H4O3,由X的分子式中可知,若3个碳原子达到饱和状态,应含有8个H原子,现在X含有4个H原子,说明X中含有两个碳氧双键,或一个碳氧双键和一个碳碳双键,由于X是由2-甲基-1,3-丁二烯与高锰酸钾反应制得,则X不能含有碳碳双键,所以X只能含有两个碳氧双键,故X的结构简式为:![]() ,能与乙醇发生酯化反应,生成酯和水,方程式为:
,能与乙醇发生酯化反应,生成酯和水,方程式为:![]() ,故答案为:
,故答案为:![]() ,
,![]() 。
。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案【题目】氮的氧化物是大气的主要污染物,是当前环保工作的重要研究内容之一。
(1)氨气还原氮的氧化物
①N2(g)+O2(g)=2NO(g) △H1
②4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H2
则4NH3(g)+6NO(g)=5N2(g)+6H2O(1) △H=_______________。(用含△H1、△H2的式子表示)
依据反应②,可将氨气直接用于燃料电池,用KOH溶液作电解质溶液,写出负极电极反应式:______________________________________________________。
(2)一定温度下,向2L恒容密闭容器中充入4.0mol NO2和4.0mol CO,在催化剂作用下发生反应4CO(g)+2NO2(g) ![]() N2(g)+4CO2(g) △H<0,测得相关数据如下:
N2(g)+4CO2(g) △H<0,测得相关数据如下:
0min | 5min | 10min | 15min | 20min | |
c(NO2)/mol/L | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
c(N2)/mol/L | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
①0~5min,用NO2的浓度变化表示的反应速率为_________________。
②以下表述能说明该反应己达到平衡状态的是________。
A.气体颜色不再变化 B.气体密度不再变化 C.气体平均相对分子质量不再变化
③20 min时,保持温度不变,继续向该容器中加入l.0mol NO2和l.0molCO,在t1时反应再次达到平衡,则NO2的转化率比原平衡_______(填“增大”、“减小”或“不变)。
④该温度下反应的化学平衡常数K= _________________。
(3)湿法脱硝:采用NaClO2 溶液作为吸收剂可对烟气进行脱硝。323 K 下,向足量碱性NaClO2 溶液中通入含NO 的烟气,充分反应后,溶液中离子浓度的分析结果如下表:
离子 | NO3- | NO2- | Cl- |
c/(mol L-1) | 2.0×10-4 | 1.0×10-4 | 1.75×10-4 |
依据表中数据,写出NaClO2溶液脱硝过程中发生总反应的离子方程式______________________。