题目内容
【题目】某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质。
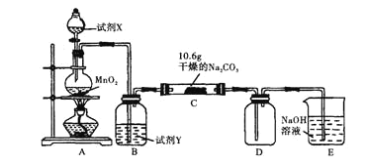
(1)写出装置A中发生反应的化学方程式:______。
(2)写出试剂Y的名称:______。
(3)已知:通入一定量的氯气后,测得D中只有一种常温下为黄红色的气体,其为含氯氧化物。充分反应后C中固体可能含有NaHCO3、NaCl、Na2CO3,为确定C中固体成分现设计如下实验:
步骤1:取C中少量固体样品于试管中,滴加足量蒸馏水至固体溶解,然后将所得溶液分别置于A、B试管中。
步骤2:向A试管中滴加过量的稀HNO3溶液,产生大量气泡,_____(填能或不能)确定碳酸钠存在,再滴加AgNO3溶液,产生白色沉淀。
步骤3:向B试管中滴加BaCl2溶液,无明显现象。
则C中固体一定含_____,一定不含_____。
(4)已知C中有0.1molCl2参加反应,由(3)已知和结论,可推知C中反应的化学方程式为_____。
【答案】MnO2+4HCl![]() MnCl2+Cl2↑+2H2O 饱和的氯化钠溶液 不能 NaHCO3、NaCl Na2CO3 2Cl2+H2O+2Na2CO3=2 NaHCO3+ 2NaCl+Cl2O
MnCl2+Cl2↑+2H2O 饱和的氯化钠溶液 不能 NaHCO3、NaCl Na2CO3 2Cl2+H2O+2Na2CO3=2 NaHCO3+ 2NaCl+Cl2O
【解析】
本题探究的是潮湿的Cl2与Na2CO3反应得到的固体物质,开始为生成Cl2的装置,除去Cl2中的杂质后与Na2CO3反应,D是安全瓶,E中的氢氧化钠溶液为尾气的吸收装置。
(1)本题探究的是潮湿的Cl2与Na2CO3反应得到的固体物质,开始为生成Cl2的装置,实验室制取Cl2的反应为MnO2+4HCl![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)除去制备出来的Cl2中的HCl选择饱和的氯化钠溶液;
(3)充分反应后C中固体可能含有NaHCO3、NaCl、Na2CO3,将固体溶解后溶液中可能存在HCO3-、CO32-,Cl-,向A试管中滴加过量的稀HNO3溶液,产生大量气泡,可能存在HCO3-或CO32-,不能确定碳酸钠存在,再滴加AgNO3溶液,产生白色沉淀,说明存在Cl-;步骤3向B试管中滴加BaCl2溶液,无明显现象,说明不存在CO32-,综上反应后的固体中一定存在NaHCO3、NaCl,不存在Na2CO3;
(4)装置C中通入一定量的氯气后,测得D中只有一种常温下为黄红色的气体,其为含氯氧化物,设化学式为ClOx,根据化合价升降守恒有x=![]() ,可得含氯氧化物为Cl2O,那么方程式为2Cl2+H2O+2Na2CO3=2 NaHCO3+ 2NaCl+Cl2O。
,可得含氯氧化物为Cl2O,那么方程式为2Cl2+H2O+2Na2CO3=2 NaHCO3+ 2NaCl+Cl2O。

【题目】实验室用干燥而纯净的氯气和二氧化硫合成硫酰氯(SO2Cl2),原理为SO2+Cl2![]() SO2Cl2,装置如图所示(夹持仪器已省略):
SO2Cl2,装置如图所示(夹持仪器已省略):
已知有关物质的部分性质如表:
物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
SO2Cl2 | -54.1 | 69.1 | ①易与水反应,产生大量白雾 ②易分解:SO2Cl2 |
H2SO4 | 10.4 | 338 | 不易分解 |
请回答下列问题:
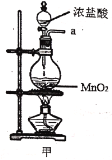
(1)写出甲中制取Cl2的化学方程式___。
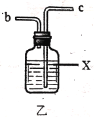
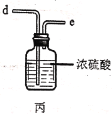
(2)利用图中甲、乙、丙装置制取干燥纯净的Cl2,并在丁装置合成硫酰氯,要完成实验目的,按气流从左到右,各接口正确的连接顺序是___。
A.abcdef B.abcedf C.acbdef D.acbedf
乙中试剂X是___。
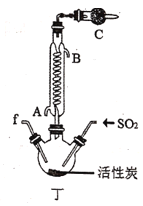
(3)丁中冷凝管进水口为___(填“A”或“B”)。装置C的作用是___。
(4)硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H=H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸。从分解产物中分离出硫酰氯的方法是___。