题目内容
4.下列各图是温度(或压强)对2A(s)+2B(g)?2C(g)+D(g)△H<0的正、逆反应速率的影响,曲线交点表示建立平衡时的温度或压强,其中正确的是( )| A. | 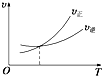 | B. |  | C. | 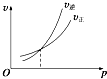 | D. | 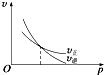 |
分析 该反应的正反应为放热反应,升高温度正逆反应速率都增大,平衡向逆反应方向移动,正反应速率小于逆反应速率,A为固体,反应物气体的化学计量数小于生成物气体的化学计量数,增大压强,平衡向逆反应方向移动,以此解答该题.
解答 解:该反应的正反应为放热反应,升高温度正逆反应速率都增大,平衡向逆反应方向移动,正反应速率小于逆反应速率,则A错误,B错误;
A为固体,反应物气体的化学计量数小于生成物气体的化学计量数,增大压强,平衡向逆反应方向移动,逆反应速率大于正反应速率,则C正确、D错误;
故选:C.
点评 本题综合考查温度、压强对反应速率和化学平衡的影响,为高考常见题型,侧重于基本理论知识的考查,注意把握反应方程式的特点,为解答该题的关键,难度不大.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
19.下列说法正确的是( )
| A. | SiH4比CH4稳定 | |
| B. | O2-半径比F-的小 | |
| C. | Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 | |
| D. | 酸性 HClO4>H2SO4>CH3COOH>H2CO3 |
15.下列变化涉及的反应类型中,属于加成反应的是( )
| A. | 苯→环已烷 | B. | 乙烯→聚乙烯 | C. | 苯→溴苯 | D. | 甲烷→四氯甲烷 |
19.将有机物完全燃烧,生成CO2和H2O.将6g该有机物的完全燃烧产物通过浓H2SO4,浓H2SO4增重7.2g,再通过碱石灰,又增重13.2g.该有机物分子式为( )
| A. | C3H8O | B. | C2H6O | C. | C2H4O2 | D. | C4H10 |
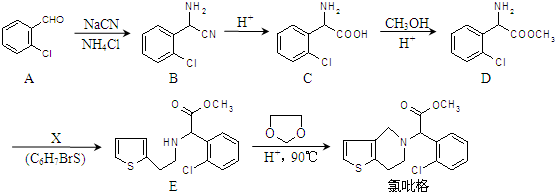
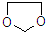 在酸性条件下生成氯吡格雷和另一种常见有机物,该有机物在浓硫酸催化下,加热脱水生成乙炔,试写出该有机物脱水生成乙炔的方程式.CH2OHCH2OH$→_{△}^{浓H_{2}SO_{4}}$CH≡CH↑+2H2O
在酸性条件下生成氯吡格雷和另一种常见有机物,该有机物在浓硫酸催化下,加热脱水生成乙炔,试写出该有机物脱水生成乙炔的方程式.CH2OHCH2OH$→_{△}^{浓H_{2}SO_{4}}$CH≡CH↑+2H2O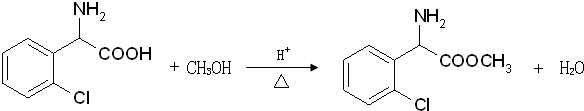
 、
、 、
、 .
.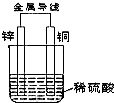 根据如图铜锌原电池示意图,回答下列问题:
根据如图铜锌原电池示意图,回答下列问题: