题目内容
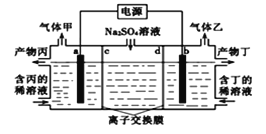
【题目】工业上常用电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为2:1,以下说法正确的是 ( )
A. b电极反应式:2H2O+4e-=O2↑+4H+
B. 离子交换膜d为阴离子交换膜
C. 丙为硫酸溶液,丁为氢氧化钠溶液
D. a电极连接电源的正极作阳极
【答案】B
【解析】
根据装置图分析可知,该装置是电解装置,电解硫酸钠溶液,实质是电解水,气体甲与气体乙的体积比约为2:1,则气体甲为氢气,气体乙为氧气,阳极生成氧气,电极反应4OH--4e-=2H2O+O2(或2H2O-4e-=O2↑+4H+),阴极生成氢气,2H++2e-=H2↑,所以判断b电极是阳极,a电极是阴极,在阳极室得到硫酸,在阴极室得到氢氧化钠,则d为阴离子交换膜,c为阳离子交换膜据此分析解答。
A、阳极b生成氧气,电极反应4OH--4e-=2H2O+O2↑(或2H2O-4e-=O2↑+4H+),故A错误;B、根据上述分析,离子交换膜d为阴离子交换膜,故B正确;C、阳极室得到硫酸,在阴极室得到氢氧化钠,所以产物丁为硫酸,丙为氢氧化钠,故C错误;D、根据上述分析,a电极是阴极,与电源负极相连,故D错误;故选B。

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目










