题目内容
有一种铁的氧化物样品,用5mol/L盐酸200mL恰好完全溶解,所得溶液还能吸收标况下2.24L氯气,恰好使其中Fe2+全部转化成Fe3+,该样品可能的化学式是( )
| A.Fe2O3 | B.Fe3O4 | C.Fe4O5 | D.Fe5O7 |
n(HCl)=0.2L×5.0mol/L=1mol,由氧化物和盐酸反应生成水可知,氧化物中含有n(O)=
n(HCl)=0.5mol,
所得溶液还能吸收0.1mol Cl2,恰好使其中的Fe2+全部转变为Fe3+,
反应后所得溶液为FeCl3,因n(Cl-)=0.2mol+1mol×2=1.2mol,
则n(Fe3+)=
n(Cl-)=0.4mol,
所以氧化物中n(Fe):n(O)=0.4:0.5=4:5,
所以化学式为Fe4O5,
故选C.
| 1 |
| 2 |
所得溶液还能吸收0.1mol Cl2,恰好使其中的Fe2+全部转变为Fe3+,
反应后所得溶液为FeCl3,因n(Cl-)=0.2mol+1mol×2=1.2mol,
则n(Fe3+)=
| 1 |
| 3 |
所以氧化物中n(Fe):n(O)=0.4:0.5=4:5,
所以化学式为Fe4O5,
故选C.

练习册系列答案
相关题目
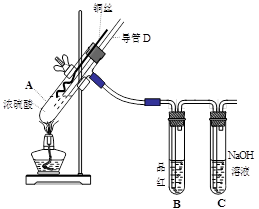
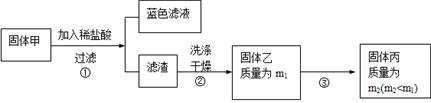 (3) 固体乙在空气中煅烧时,使用的实验仪器除了玻璃棒、三脚架、酒精灯外,还必须有: 。
(3) 固体乙在空气中煅烧时,使用的实验仪器除了玻璃棒、三脚架、酒精灯外,还必须有: 。