题目内容
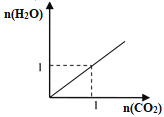
【题目】如图所示是两种气态烃组成的混合气体完全燃烧所得的CO2和H2O的物质的量(单位:mol)的变化关系。下列判断不正确的是:
A. 一定含有甲烷
B. 可能含有乙烷
C. 可能含有乙炔
D. 若120℃不变,反应前后气体体积不一定发生变化
【答案】A
【解析】
由图像可知该混合烃燃烧生成的CO2和H2O的物质的量相等,则该混合烃中碳、氢原子个数比为1:2,根据平均值的特点,有种情形:一是各组分碳、氢原子个数比都是1:2;二是两组分碳、氢原子个数比一个大于1:2,另一个小于1:2,由此分析。
A.由图像可知该混合烃燃烧生成的CO2和H2O的物质的量相等,则该混合烃中碳、氢原子个数比为1:2。该混合烃可以是两种烯烃(如乙烯和丙烯:碳、氢原子个数比均为1:2)混合物;或者是乙炔(C2H2碳、氢原子个数比大于1:2)与丙烷或丁烷(C3H8或C4H10碳、氢原子个数比均小于1:2)混合物,所以该混合烃中不一定含有甲烷,A项错误;
B.因为乙烷(C2H6)中碳、氢原子个数比为1:3(小于1:2),乙烷与乙炔(C2H2:碳、氢原子个数比大于1:2)的混合物中碳、氢原子个数比可能为1:2,所以该混合烃中可能含有乙烷,B项正确;
C.根据A、B项分析知,该混合烃中可能含有乙炔,C项正确;
D.设该混合烃的平均组成为CxHy,其燃烧通式为CxHy+(x+![]() )O2→xCO2+
)O2→xCO2+![]() H2O(g),因在1200C时水为蒸气,若使燃烧前后气体体积不变则有1+(x+
H2O(g),因在1200C时水为蒸气,若使燃烧前后气体体积不变则有1+(x+![]() )=x+
)=x+![]() ,解得y=4,即平均组成为CxH4,且同时满足碳、氢原子个数比为1:2,这两种气态烃可以是甲烷(CH4碳、氢原子个数比小于1:2)和丙炔(C3H4碳、氢原子个数比大于1:2),所以在120℃下当混合烃为甲烷和丙炔时,反应前后气体体积不发生变化,D项正确;答案选A。
,解得y=4,即平均组成为CxH4,且同时满足碳、氢原子个数比为1:2,这两种气态烃可以是甲烷(CH4碳、氢原子个数比小于1:2)和丙炔(C3H4碳、氢原子个数比大于1:2),所以在120℃下当混合烃为甲烷和丙炔时,反应前后气体体积不发生变化,D项正确;答案选A。

 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案【题目】实验室用浓盐酸、二氧化锰共热制氯气,并用制得的氯气和氢氧化钙制取少量漂粉精。现已知反应:2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O是放热反应。温度稍高会发生副反应:6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O。
现有3个同学分别设计的3套实验装置如图:

(1)C装置中发生反应的化学方程式为:___,E装置中发生反应的化学方程式为:___。
(2)请从以下几个方面对甲乙丙3套实验装置的优缺点作出评价,并将符合题目要求的选项的序号填在表中空格中。___
a.不容易控制反应速率 b.容易控制反应速率
c.有副反应发生 d.可防止副反应发生
e.污染环境 f.可防止污染环境
优点 | 缺点 | |
甲装置 | ||
乙装置 | ||
丙装置 |
(3)上述装置中甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G两部分组成,请从上述装置中选取合理的部分,组装一套较完整的实验装置,装置各部分的连接顺序是___(按气流流动的方向)。该组合中还缺少的装置是___(用文字说明),需要该装置的原因是___。
(4)实验室若用16mol/L的盐酸100mL与足量的二氧化锰反应,理论上最终生成的次氯酸钙的物质的量最多不超过___mol。








