题目内容
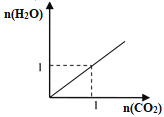
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列说法不正确的是:

A. 电池工作时,CO32-向电极A移动
B. 电极A上H2参与的电极反应:H2-2e-=2H+
C. 电极B上发生电极反应:O2+2CO2+4e-=2CO32-
D. 反应CH4+H2O=3H2+CO,每消耗22.4 L CH4气体,转移6 mol e-
【答案】D
【解析】
由电池原理示意图看出,CH4和水蒸气经过催化重整后生成CO和H2,CO和H2通入燃料电池A极,电池放电后生成CO2和H2O,由碳元素化合价由CO中的+2价变化到CO2中的+4价,失去电子,因此A极是电池的负极;B极通入O2和CO2,O2作氧化剂,O2+4e-+2CO2=2CO32-,B为正极。由此分析。
A.燃料电池属于原电池,A极为负极,原电池工作时阴离子向负极迁移,即CO32-向A极移动,A项正确;
B.由电池原理示意图看出,A极通入CO和H2,电池放电后生成CO2和H2O,所以H2参与的电极反应为:H2-2e-=2H+,H+再与CO32-发生离子反应:2H++CO32-=CO2↑+H2O,B项正确;
C.由电池原理示意图看出,电极B通入O2和CO2,作电池正极,发生还原反应,所以电极反应为O2+2CO2+4e-=2CO32-,C项正确;
D.CH4和水蒸气经过催化重整生成CO和H2,发生反应CH4+H2O![]() 3H2+CO,碳元素的化合价由CH4中的-4价变化到CO中的+2价,化合价升高6价,即每个碳原子失去6个电子,由于题目未明确22.4LCH4气体是否处于标准状况,无法确定22.4LCH4气体的物质的量,所以无法计算每消耗22.4LCH4气体时转移电子的物质的量,D项错误;答案选D。
3H2+CO,碳元素的化合价由CH4中的-4价变化到CO中的+2价,化合价升高6价,即每个碳原子失去6个电子,由于题目未明确22.4LCH4气体是否处于标准状况,无法确定22.4LCH4气体的物质的量,所以无法计算每消耗22.4LCH4气体时转移电子的物质的量,D项错误;答案选D。

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目