题目内容
【题目】N2O俗名为“笑气”,也是一种温室气体。结合所学知识,回答下列问题:
(1)锌与极稀硝酸反应可生成N2O,该反应的化学方程式为___________,其中作氧化剂的硝酸与参与反应的硝酸的物质的量之比为___________。
(2)已知几种物质的相对能量如下:
物质 | N2O(g) | CO(g) | N2(g) | CO2(g) |
相对能量/kJmol-1 | 475.5 | 283.0 | 393.5 | 0 |
①N2O(g)和CO(g)反应生成N2(g)和CO2(g)的热化学方程式为____________。
②若其他条件不变,加入高效催化剂,该反应的焓变将_______(填“增大”、“减小”或“不变”)。
(3)碘蒸气能催化N2O的分解,反应历程(步骤)如下:
i.I2(g)2I(g)
ii.I(g)+N2O(g)=N2(g)+IO(g)
iii.2IO(g)+2N2O(g)=2N2(g)+2O2(g)+I2(g)
实验表明,在反应过程c(I)始终大于c(IO),由此推测,反应速率ii_________iii(填“>”、“<”或“=”)。
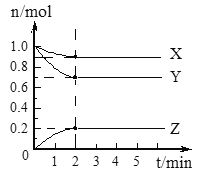
(4)一定温度下,向恒容密闭容器中充入2 mol N2O(g)和3 mol NO(g),发生反应:N2O(g)+NO(g)N2(g)+NO2(g) △H。测得N2体积分数与温度、时间的关系如图所示。

①△H___________0(填“>”、“<”或“=”)。
②下列情况表明该反应达到平衡状态的是___________(填字母)。
A.混合气体的密度不再改变 B.相对分子质量不再改变
C.NO和NO2的消耗速率相等 D.N2O的体积分数不再改变
③T1时,该反应的平衡常数K=___________。
【答案】4Zn+10HNO3=4Zn(NO3)2+N2O![]() +5H2O 1:5 N2O(g)+CO(g)=N2(g)+CO2(g) H=-365.0kJmol-1 不变 < < CD 3
+5H2O 1:5 N2O(g)+CO(g)=N2(g)+CO2(g) H=-365.0kJmol-1 不变 < < CD 3
【解析】
锌与极稀硝酸反应生成N2O,发生氧化还原反应;H=生成物的总能量-反应物的总能量;由N2体积分数与温度、时间的关系图象可知,T1温度下,先达到平衡,说明T1>T2。
(1)锌与极稀硝酸反应生成N2O,氮元素化合价降低,锌元素化合价升高生成硝酸锌,根据电子守恒得反应方程式4Zn+10HNO3=4Zn(NO3)2+N2O![]() +5H2O。硝酸表现氧化性和酸性,表现氧化性的硝酸生成N2O,表现酸性的生成Zn(NO3)2,故作氧化剂的硝酸与参与反应的硝酸的物质的量之比为1:5。
+5H2O。硝酸表现氧化性和酸性,表现氧化性的硝酸生成N2O,表现酸性的生成Zn(NO3)2,故作氧化剂的硝酸与参与反应的硝酸的物质的量之比为1:5。
(2)①N2O(g)和CO(g)反应生成N2(g)和CO2(g),H=生成物的总能量-反应物的总能量=(0+393.5-283.0-475.5)kJmol-1=-365.0 kJmol-1,热化学方程式为N2O(g)+CO(g)=N2(g)+CO2(g) H=-365.0kJmol-1。
②催化剂不影响焓变,故加入高效催化剂,该反应的焓变不变。
(3)反应ii消耗I(g)生成IO(g),反应iii消耗IO(g),因实验表明,在反应过程c(I)始终大于c(IO),故反应速率ii<iii。
(4) ①由图可知,T1>T2,T1温度下平衡时N2体积分数小于T2温度下平衡时N2体积分数,说明温度升高,平衡逆向移动,故正反应为放热反应,△H<0。
②A.该反应中,生成物和反应物均为气体,气体的总质量不变,容器体积不变,故平衡前后气体密度始终不变,A错误;
B.反应前后气体分子数相等,气体总质量不变,故相对分子质量始终不变,B错误;
C.NO和NO2的消耗速率相等,说明正逆反应速率相等,反应达到平衡,C正确; D.N2O的体积分数不再改变,说明反应达到平衡,D正确;
答案选CD。
③反应前后气体分子数不变,气体总物质的量为5mol,T1温度下,平衡时N2体积分数为30%,n(N2)=1.5mol,n(NO2)=1.5mol,n(N2O)=0.5mol,n(NO)=1.5mol,设体积V=1,K= ![]() 。
。

 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案