题目内容
【题目】Hagrmann酯(H)是一种合成多环化合物的中间体,可由下列路线合成(部分反应条件略去):
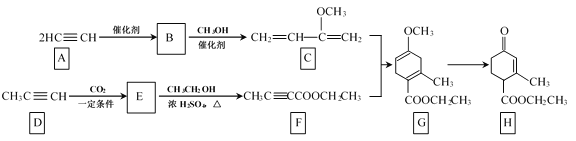
(1)B的结构简式是__;B→C的反应类型是__;H中含有的官能团名称是羰基、___。
(2)E→F的化学方程式是___。
(3)TMOB是H的同分异构体,具有下列结构特征:
①除苯环外仅有1种化学环境的H原子;
②存在甲氧基(CH3O—)。
TMOB的结构简式是___。
(4)下列说法正确的是__。
a.A能和HCl反应得到聚氯乙烯的单体
b.D和F中均含有2个不饱和度
c.1molG完全燃烧生成7molH2O
d.H能发生加成、取代反应
(5)请写出乙炔和HCHO为有机原料合成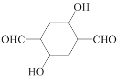 的合成路线图___(无机试剂任选)。
的合成路线图___(无机试剂任选)。
已知:①—C![]() CH+
CH+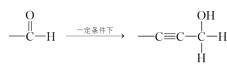
②—CHO+
(合成路线常用的表示方式为:A![]() B
B![]() ……目标产物)
……目标产物)
【答案】H![]() C-CH=CH2 加成反应 酯基,碳碳双键 CH3C
C-CH=CH2 加成反应 酯基,碳碳双键 CH3C![]() C—COOH+CH3CH2OH
C—COOH+CH3CH2OH![]() CH3C
CH3C![]() C—COOCH2CH3+H2O
C—COOCH2CH3+H2O ![]() ad CH
ad CH![]() CH
CH![]() HO—CH2—C
HO—CH2—C![]() C—CH2—OH
C—CH2—OH![]() HO—CH2—CH2—CH2—CH2—OH
HO—CH2—CH2—CH2—CH2—OH![]() OHC—CH2—CH2—CHO
OHC—CH2—CH2—CHO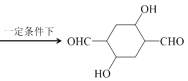
【解析】
(1)A→B为两个乙炔分子进行加成反应得到B(H![]() C-CH=CH2),然后继续与甲醇加成得到C;根据H的结构简式可知,分子中含有的官能团名称是羰基、酯基、碳碳双键;
C-CH=CH2),然后继续与甲醇加成得到C;根据H的结构简式可知,分子中含有的官能团名称是羰基、酯基、碳碳双键;
(2)E→F是酯化反应,根据F的结构简式可知E的结构简式为CH3C![]() C-COOH,反应的化学方程式是:CH3C
C-COOH,反应的化学方程式是:CH3C![]() C-COOH+CH3CH2OH
C-COOH+CH3CH2OH![]() CH3C
CH3C![]() C-COOCH2CH3+H2O;
C-COOCH2CH3+H2O;
(3)TMOB的结构中除苯环外只有一个吸收峰且存在—OCH3;H中共有3个O,故TMOB有3个—OCH3结构;又因为还有一个C,故三个—OCH3结构连在一个C上,即该物质的结构简式为![]() ;
;
(4) a.A能和HCI反应生成氯乙烯,氯乙烯加聚即得到聚氯乙烯,a正确;
b.根据结构简式可判断D中含有2个不饱和度,而F中含有3个不饱和度,b不正确;
c.G的分子式为C11H16O3,则1 mol G完全燃烧生成8mol H2O,c不正确;
d.H分子中的羰基和碳碳双键均能发生加成,酯基和饱和碳原子上的氢原子可以发生取代反应,d正确,
答案选ad;
(5)根据已知信息结合逆推法可知乙炔和HCHO合成 的路线图如下:CH
的路线图如下:CH![]() CH
CH![]() HO—CH2—C
HO—CH2—C![]() C—CH2—OH
C—CH2—OH![]() HO—CH2—CH2—CH2—CH2—OH
HO—CH2—CH2—CH2—CH2—OH![]() OHC—CH2—CH2—CHO
OHC—CH2—CH2—CHO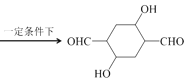 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】N2O俗名为“笑气”,也是一种温室气体。结合所学知识,回答下列问题:
(1)锌与极稀硝酸反应可生成N2O,该反应的化学方程式为___________,其中作氧化剂的硝酸与参与反应的硝酸的物质的量之比为___________。
(2)已知几种物质的相对能量如下:
物质 | N2O(g) | CO(g) | N2(g) | CO2(g) |
相对能量/kJmol-1 | 475.5 | 283.0 | 393.5 | 0 |
①N2O(g)和CO(g)反应生成N2(g)和CO2(g)的热化学方程式为____________。
②若其他条件不变,加入高效催化剂,该反应的焓变将_______(填“增大”、“减小”或“不变”)。
(3)碘蒸气能催化N2O的分解,反应历程(步骤)如下:
i.I2(g)2I(g)
ii.I(g)+N2O(g)=N2(g)+IO(g)
iii.2IO(g)+2N2O(g)=2N2(g)+2O2(g)+I2(g)
实验表明,在反应过程c(I)始终大于c(IO),由此推测,反应速率ii_________iii(填“>”、“<”或“=”)。
(4)一定温度下,向恒容密闭容器中充入2 mol N2O(g)和3 mol NO(g),发生反应:N2O(g)+NO(g)N2(g)+NO2(g) △H。测得N2体积分数与温度、时间的关系如图所示。
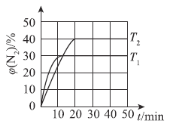
①△H___________0(填“>”、“<”或“=”)。
②下列情况表明该反应达到平衡状态的是___________(填字母)。
A.混合气体的密度不再改变 B.相对分子质量不再改变
C.NO和NO2的消耗速率相等 D.N2O的体积分数不再改变
③T1时,该反应的平衡常数K=___________。
【题目】下列实验的现象与对应结论均正确的是
选项 | 操作 | 现象 | 结论 |
A | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
B | 向某溶液中逐滴加入盐酸 | 产生无色无味气体 | 此溶液中含有 |
C | 向某溶液中滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无 |
D | 先向某溶液中逐滴加入氯化钡溶液,再加稀硝酸 | 有白色沉淀产生,且沉淀不溶解 | 此溶液中一定含有 |
A.AB.BC.CD.D