题目内容
4.中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是( )| 选项 | 规律 | 结论 |
| A | 强氧化性物质可以用来杀菌消毒 | ClO2可用于自来水消毒 |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硫酸,浓硫酸中铝片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | NH3沸点低于PH3 |
| D | 较强的酸可以制取较弱的酸 | 硫化氢通入硫酸铜溶液中不能反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、强氧化性物质能使蛋白质变性而杀菌消毒;
B、铝在冷浓硫酸中发生钝化;
C、NH3分子之间存在氢键;
D、是因为复分解反应生成难溶于硫酸的硫化铜.
解答 解:A、强氧化性物质能使蛋白质变性而杀菌消毒,ClO2具有强氧化性,可以杀菌消毒,故A正确;
B、铝在冷浓硫酸中发生钝化,表面形成致密的氧化膜,而阻止酸与铝的接触,所以反应速度变慢,故B错误;
C、NH3分子之间存在氢键,使物质的熔沸点升高,所以氨气的沸点比磷化氢的沸点高,故C错误;
D、硫化氢通入硫酸铜溶液中,生成难溶于硫酸的硫化铜,符合复分解反应的条件,使反应得以发生,与强制弱无关,故D错误;
故选A.
点评 本题考查物质的用途,明确物质的性质是解本题关键,性质决定用途,注意二氧化硅虽然属于酸性氧化物,但能和HF反应,注意二氧化硫漂白性和次氯酸漂白性的区别,题目难度不大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
8. 25℃时在10mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )
25℃时在10mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )
 25℃时在10mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )
25℃时在10mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )| A. | 当溶液的pH=8时,溶液中NaHCO3的物质的量浓度为0.1mol/L | |
| B. | HCl溶液滴加一半时,溶液pH>7 | |
| C. | 0.1mol/LNa2CO3溶液中c(Na+)+c(H+)=c(OH-)+2c(CO32-)+c(HCO3-) | |
| D. | 在M点:c(Na+)>c(CO32-)=c(HCO3-)>c(OH-)>c(H+) |
15.将铁屑溶于过量盐酸后,再加入下列物质,不会有三价铁生成的是( )
| A. | 过氧化氢 | B. | 氯水 | C. | 硝酸锌 | D. | 氯化铜 |
12.从实验测得不同物质中氧氧之间的键长和键能的数据:
其中x、y的键能数据尚未测定,但可根据规律性推导键能的大小顺序为w>z>y>x;该规律性是( )
| O-O键 数据 | O22- | O2- | O2 | O2+ |
| 键长(10-12 m) | 149 | 128 | 121 | 112 |
| 键能(kJ•mol-1) | x | y | z=494 | w=628 |
| A. | 成键的电子数越多,键能越大 | B. | 键长越长,键能越小 | ||
| C. | 成键所用的电子数越少,键能越大 | D. | 成键时电子对越偏移,键能越大 |
19.在一定条件下,动植物油脂与醇反应可制备生物柴油,化学方程式如下:
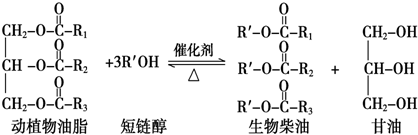
下列叙述错误的是( )

下列叙述错误的是( )
| A. | 生物柴油由可再生资源制得 | B. | 生物柴油是不同酯组成的混合物 | ||
| C. | 动植物油脂是高分子化合物 | D. | “地沟油”可用于制备生物柴油 |
9.下列说法中,正确的是( )
| A. | 中和反应反应热的测定实验中,将环形玻璃搅拌棒换成环形铜丝搅拌棒测定出来的中和热值偏大 | |
| B. | 在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-571.6KJ/mol | |
| C. | 将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6KJ/mol | |
| D. | HCl和NaOH反应的中和热△H=-57.3KJ/mol,则H2SO4和Ca(OH)2反应的反应热△H=-(2×57.3)KJ/mol |
13.下列有机物系统命名正确的是( )
| A. |  2-乙基丙烷 2-乙基丙烷 | B. | CH3CH2CH2CH2OH 1-丁醇 | ||
| C. |  对二甲苯 对二甲苯 | D. |  2-甲基-2-丙烯 2-甲基-2-丙烯 |
14.阿波罗号宇宙飞船上使用的氢氧燃料电池,其电池反应为:2H2+O2=2H2O,电解质溶液为KOH溶液,反应保持在较高温度 ,使H2O蒸发,则下列叙述中正确的是( )
| A. | 此电池能发生蓝色火焰 | |
| B. | H2为正极,O2为负极 | |
| C. | 工作时,电解质溶液的pH不断减小 | |
| D. | 电极反应分别为负极:2H2+4 OH--4e-=4 H2O;正极:O2+2 H2O+4e-=4 OH- |
