题目内容
3.常温下,稀释0.1mol•L-1Na2CO3溶液,图中的纵坐标可以表示( )
| A. | 溶液中HCO3-的数目 | B. | 溶液的pH | ||
| C. | CO32- 水解的平衡常数 | D. | 溶液中的c(CO32-) |
分析 A、加水稀释,碳酸根离子水解平衡正移;
B、加水稀释,溶液中氢氧根离子浓度减小;
C、水解的平衡常数只与温度有关;
D、稀释过程中水解平衡CO32-+H2O?HCO3-+OH-向右移动,所以HCO3-数目增大,CO32-数目减少.
解答 解:A、加水稀释,碳酸根离子水解平衡正移,溶液中HCO3-的数目,故A正确;
B、加水稀释,溶液的体积增大,溶液中氢氧根离子浓度减小,所以稀释过程中溶液pH应逐渐减小,故B错误;
C、水解的平衡常数只与温度有关,加水稀释平衡常数不变,故C错误;
D、稀释过程中水解平衡CO32-+H2O?HCO3-+OH-向右移动,所以HCO3-数目增大,CO32-数目减少,所以c(CO32-)减小,故DD错误;
故选A.
点评 本题考查了影响盐类水解的因素,水解平衡常数只受温度影响,本题难度不大.

练习册系列答案
相关题目
8.下列说法不正确的是( )
| A. | Na2CO3溶液中c(Na+)与c(CO32-)之比大于2:1 | |
| B. | 蒸发氯化铝溶液要不断通入氯化氢气体方可得到氯化铝晶体 | |
| C. | 1 L 0.3 mol/L醋酸溶液中H+个数与3 L 0.1 mol/L醋酸溶液中H+个数之比为1:1 | |
| D. | 浓度相同的下列溶液中,按pH由小到大的顺序排列的是CH3COONa、NaHCO3、Na2CO3 |
13.下列关于有机物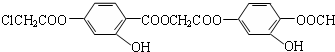 的说法,正确的是( )
的说法,正确的是( )
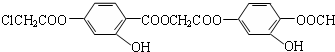 的说法,正确的是( )
的说法,正确的是( )| A. | 该有机物分子中含有氯原子、羟基、羧基等官能团 | |
| B. | 1mol该化合物最多可与10molNaOH反应 | |
| C. | 该有机物在酸性条件下水解,生成的有机物只有两种 | |
| D. | 该有机物可与浓溴水发生加成反应,但不能发取代去反应 |
 NO2+3H2$\stackrel{140℃}{→}$
NO2+3H2$\stackrel{140℃}{→}$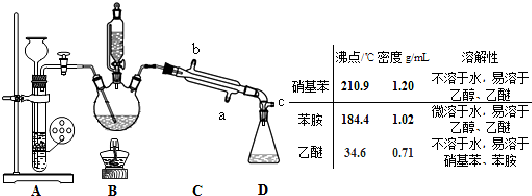
 +4MnO2+5H2SO4→2
+4MnO2+5H2SO4→2 +4MnSO4+1(NH4)2SO4+4H2O.
+4MnSO4+1(NH4)2SO4+4H2O.
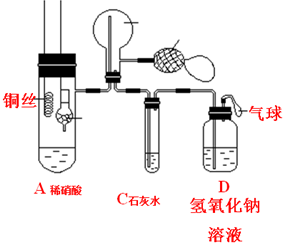
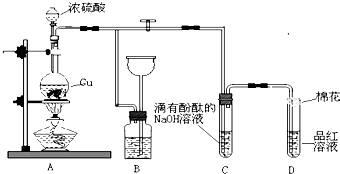
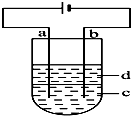 由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.应用如图所示电解实验可制得白色纯净的Fe(OH)2沉淀.两电极的材料分别为石墨和铁.
由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.应用如图所示电解实验可制得白色纯净的Fe(OH)2沉淀.两电极的材料分别为石墨和铁.