题目内容
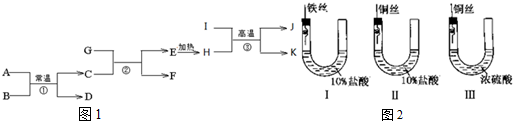
13.如图是一种合成 路线:
路线:已知以下信息:
①有机化合物A可用来衡量一个国家石油化学工业发展水平.
②有机化合物C的核磁共振氢谱显示其有3种不同化学环境的氢原子.
③

根据上述信息回答下列问题:
(1)A的结构式是
 .
.(2)B的结构简式为CH3CH2OH.
(3)C生成D的化学方程式为
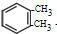 +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$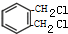 +2HCl
+2HCl(4)反应Ⅱ的试剂是氢氧化钠水溶液,该反应类型为取代反应.
(5)在G的同分异构体中,既能与新制的Cu(OH)2悬浊液在加热条件下反应生成砖红色沉淀,又能与碳酸钠反应生成二氧化碳,还能使FeCl3溶液显色的有
10种,所有这些同分异构体中,不同化学环境氢原子的种数相同(填“相同”“不相同”).

分析 由邻苯二甲酸二乙酯结构可知,邻苯二甲酸和乙醇发生酯化反应生成,有机化合物A可用来衡量一个国家石油化学工业发展水平,A为乙烯,CH2=CH2中含有不饱和的C=C双键,能够在催化剂存在条件下与水发生加成反应生成乙醇CH3CH2OH,则B为乙醇,G为邻苯二甲酸 ,含几种位置的H原子,则核磁共振氢谱就有几种,有机化合物C化学式为C8H10,核磁共振氢谱显示有3种不同化学环境的氢原子,说明含有3种氢原子,则C为
,含几种位置的H原子,则核磁共振氢谱就有几种,有机化合物C化学式为C8H10,核磁共振氢谱显示有3种不同化学环境的氢原子,说明含有3种氢原子,则C为 ,与氯气发生取代反应生成D为
,与氯气发生取代反应生成D为 ,F能发生银镜反应,说明F为醛,且G为邻苯二甲酸,所以F
,F能发生银镜反应,说明F为醛,且G为邻苯二甲酸,所以F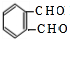 ,则E→F为醇的催化氧化,所以E为
,则E→F为醇的催化氧化,所以E为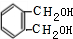 ,D→E为卤代烃的取代反应,据此分析解答.
,D→E为卤代烃的取代反应,据此分析解答.
解答 解:由邻苯二甲酸二乙酯结构可知,邻苯二甲酸和乙醇发生酯化反应生成,有机化合物A可用来衡量一个国家石油化学工业发展水平,A为乙烯,CH2=CH2中C=C双键,其中1个C-C断裂结合水提供的-H、-OH,发生加成反应,反应的化学方程式为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,生成乙醇CH3CH2OH,则B为乙醇,G为邻苯二甲酸 ,有机化合物C化学式为C8H10,核磁共振氢谱显示有3种不同化学环境的氢原子,说明含有3种氢原子,则C为
,有机化合物C化学式为C8H10,核磁共振氢谱显示有3种不同化学环境的氢原子,说明含有3种氢原子,则C为 ,与氯气发生取代反应
,与氯气发生取代反应 +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$ +2HCl,生成D为
+2HCl,生成D为 ,F能发生银镜反应,说明F为醛,且G为邻苯二甲酸,所以F
,F能发生银镜反应,说明F为醛,且G为邻苯二甲酸,所以F ,则E→F为醇的催化氧化
,则E→F为醇的催化氧化 +O2$→_{△}^{催化剂}$
+O2$→_{△}^{催化剂}$ +2H2O,所以E为
+2H2O,所以E为 ,D→E为卤代烃的取代反应:
,D→E为卤代烃的取代反应: +2H2O$→_{△}^{NaOH的水溶液}$
+2H2O$→_{△}^{NaOH的水溶液}$ +2HCl,
+2HCl,
(1)根据分析可知,A为CH2=CH2,乙烯的结构式为: ,故答案为:
,故答案为: ;
;
(2)由邻苯二甲酸二乙酯结构可知,邻苯二甲酸和乙醇发生酯化反应生成,则B为乙醇,结构简式为CH3CH2OH,故答案为:CH3CH2OH;
(3)有机化合物C化学式为C8H10,核磁共振氢谱显示有3种不同化学环境的氢原子,说明含有3种氢原子,则C为 ,与氯气发生取代反应,反应方程式为:
,与氯气发生取代反应,反应方程式为: +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$ +2HCl,
+2HCl,
故答案为: +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$ +2HCl;
+2HCl;
(4)D→E为卤代烃的取代反应: +2H2O$→_{△}^{NaOH的水溶液}$
+2H2O$→_{△}^{NaOH的水溶液}$ +2HCl,所以反应Ⅱ的试剂是氢氧化钠水溶液,
+2HCl,所以反应Ⅱ的试剂是氢氧化钠水溶液,
故答案为:氢氧化钠水溶液;取代反应;
(5)G为邻苯二甲酸 ,满足下列条件的同分异构体:能与新制的Cu(OH)2悬浊液混合加热生成砖红色沉淀,含有醛基,又能与碳酸钠反应生成二氧化碳,含有羧基,能与FeCl3溶液发生显色反应,含有酚羟基;说明苯环上有-OH、-CHO、-COOH三个取代基,-OH、-CHO处于邻位,-COOH有4种位置,-OH、-CHO处于间位,-COOH有4种位置,-OH、-CHO处于对位,-COOH有2种位置,有10种;所有这些同分异构体中,不同化学环境氢原子的种数都为6种,
,满足下列条件的同分异构体:能与新制的Cu(OH)2悬浊液混合加热生成砖红色沉淀,含有醛基,又能与碳酸钠反应生成二氧化碳,含有羧基,能与FeCl3溶液发生显色反应,含有酚羟基;说明苯环上有-OH、-CHO、-COOH三个取代基,-OH、-CHO处于邻位,-COOH有4种位置,-OH、-CHO处于间位,-COOH有4种位置,-OH、-CHO处于对位,-COOH有2种位置,有10种;所有这些同分异构体中,不同化学环境氢原子的种数都为6种,
故答案为:10;相同.
点评 本题考查有机物的推断,题目难度中等,注意根据有机物分子式、反应条件以及题目给予的反应信息进行推断,熟练有机物官能团性质与转化是关键,试题培养了学生的分析、理解能力及逻辑推理能力.

 名校课堂系列答案
名校课堂系列答案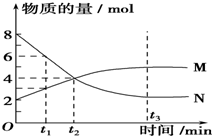
| A. | 化学方程式为:2M?N | B. | t3时,正逆反应速率相等 | ||
| C. | t3时,正反应速率大于逆反应速率 | D. | t1时,N的浓度是M浓度的3倍 |
| 序号 | 物质 | 试剂 | 除杂方法 |
| ① | 甲烷(C2H4) | ||
| ② | 溴苯?(溴) |
| A. | 取代-消去-加成-氧化 | B. | 消去-加成-取代-氧化 | ||
| C. | 消去-取代-加成-氧 | D. | 取代-加成-氧化-消去 |
| A. | 0.1 mol•L-1Ca(NO3)2溶液中:Na+、N${{H}_{4}}^{+}$、C${{O}_{3}}^{2-}$、CH3COO- | |
| B. | 能使甲基橙变红的溶液中:K+、Na+、N${{O}_{3}}^{-}$、Cl- | |
| C. | 3%H2O2溶液中:Fe2+、H+、S${{O}_{4}}^{2-}$、Cl- | |
| D. | 0.1 mol•L-1KSCN溶液中:Fe3+、N${{H}_{4}}^{+}$、Br-、S${{O}_{4}}^{2-}$ |
C2H5OH(g)═C2H5OH(l)△H2=-b kJ/mol
H2O(g)═H2O(l)△H3=-c kJ/mol
若使92g酒精液体完全燃烧,最后恢复到室温,则放出的热量(单位kJ)为( )
| A. | 4a+4b+4c | B. | 2a-2b+6c | C. | 2a-2b+2c | D. | 2a-6b+2c |
| A. | 澄清的石灰水,浓硫酸 | B. | 浓硫酸,溴水 | ||
| C. | 溴水,浓硫酸 | D. | 浓硫酸,酸性KMnO4溶液 |
| A. | 甲烷 | B. | 乙烯 | C. | 乙烷 | D. | 苯 |
 ,F的电子式为
,F的电子式为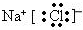 .
.