题目内容
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是( )
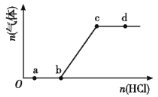
A.a点对应的溶液中:Na+、OH-、SO42-、NO3-
B.b点对应的溶液中:K+、Ca2+、H+、Cl-
C.c点对应的溶液中:Na+、Ca2+、NO3-、Cl-
D.d点对应的溶液中:F-、NO3-、Fe2+、Ag+
【答案】C
【解析】
A. a点对应的溶液中含有碳酸氢钠,HCO3-、OH-反应生成CO32-和水,a点对应的溶液中不能有大量OH-,故不选A;
B. b点对应的溶液中有碳酸氢钠,HCO3-、H+反应生成CO2气体和水,b点对应的溶液中不能有大量H+,故不选B;
C. c点对应的溶液中溶质只有氯化钠,Na+、Ca2+、NO3-、Cl-不反应,能共存,故选C;
D. d点对应的溶液中含有盐酸, F-、H+反应生成弱酸HF,H+、NO3-、Fe2+发生氧化还原反应生成Fe3+,Ag+、Cl-反应生成氯化银沉淀,不能大量共存,故不选D;答案选C。

【题目】汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NOx等有毒气体,其污染问题也成为当今社会急需解决的问题。
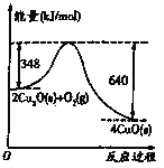
(1)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图:

则该反应的热化学方程式为_____________________________。
(2)对汽车加装尾气净化装置,可使CO、NOx有毒气体相互反应转化为无毒气体。
2xCO+2NOx ="=" 2xCO2+N2,当转移电子物质的量为0.4x mol时,该反应生成标准状况下的N2体积_____________________L。
(3)一氧化碳是一种用途相当广泛的化工基础原料。可以还原金属氧化物,还可以用来合成很多有机物如甲醇等。在压强为0.1 MPa条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下反应生成甲醇: CO(g)+2H2(g)![]() CH3OH(g);△H= -b kJmol-1
CH3OH(g);△H= -b kJmol-1
①该反应的平衡常数表达式为_____________________________。
②若容器容积不变,下列措施可增加甲醇产率的是______________
A.升高温度 | B.将CH3OH(g)从体系中分离 |
C.充入He,使体系总压强增大 | D.再充入1 mol CO和3 mol H2 |
③经测定不同温度下该反应的平衡常数如下:
温度(℃) | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO) =0.4 mol/L、c(H2)=0.4 mol/L、c(CH3OH)=0.8 mol·L-1, 则此时v正___________v逆(填>、<或=)。
(4)甲醇是重要的基础化工原料,又是一种新型的燃料,最近有人制造了一种燃料电池,一个电极通入空气,另一个电极加入甲醇,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-离子。该电池的正极反应式为_____________________________。电池工作时,固体电解质里的O2-向_______极移动。