题目内容
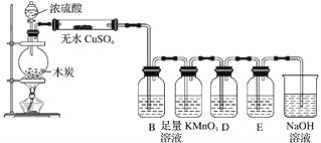
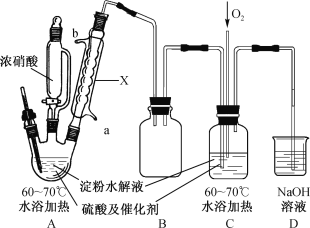
【题目】某实验小组制备草酸晶体(H2C2O4·2H2O)的实验装置如下:
已知:I.草酸(H2C2O4)是二元弱酸,熔点101~102℃;
II.草酸的溶解度如下表所示:
温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度/g·(100g水)-1 | 9.5 | 14.3 | 21.2 | 31.4 | 46.0 | 84.5 |
III.在催化剂和硫酸存在下,用浓硝酸氧化淀粉水解液可制备草酸,发生的主要反应为:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O。
回答下列问题:
(1)装置A中仪器X名称为___________,水从接口___________(填“a”或“b”)进入。
(2)装置B的作用是___________;设计装置C的目的是_________________________。
(3)反应C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O中,每生成1 mol H2C2O4转移电子的物质的量为____________。
(4)将装置A和C中反应液浓缩、静置结晶并过滤得粗草酸晶体,提纯H2C2O4·2H2O的方法是_________________________。
(5)探究草酸的性质:
①向Na2CO3溶液中滴加H2C2O4溶液,产生大量气体,说明草酸的酸性比碳酸________(填“强”或“弱”)。
②向NaClO溶液中加入过量H2C2O4溶液,有气泡产生,能解释这一现象的离子方程式为___。
【答案】(球形)冷凝管 a 安全瓶 提高HNO3的利用率 6mol 重结晶 强 ClO-+H2C2O4= Cl-+2CO2↑+H2O
【解析】
(1)装置A中仪器X名称为(球形)冷凝管,冷却水流向都是下进上出。
(2)装置B中两导管都短,主要是防止倒吸;在装置C中,NO、NO2、O2反应生成HNO3,能将淀粉水解液中的葡萄糖氧化为草酸。
(3)反应C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O中,有机物中C元素价态不一定相同,计算变价数比较麻烦,当然也可从平均化合价进行分析,还可从N元素的价态变化判断电子转移的数目。
(4)装置A和C最终都发生葡萄糖氧化为酸的反应,最终所得溶液中都含草酸,从粗草酸晶体提纯H2C2O4·2H2O的方法是溶解后再结晶。
(5)①向Na2CO3溶液中滴加H2C2O4溶液,产生大量气体,应为CO2,反应满足强酸制弱酸的原则。
②向NaClO溶液中加入过量H2C2O4溶液,有气泡产生,则生成CO2,ClO-被还原为Cl-。
(1)装置A中仪器X名称为(球形)冷凝管,冷却水从接口a进入。答案为:(球形)冷凝管;a;
(2)装置B主要是为了防止倒吸,其作用为安全瓶;设计装置C的目的是将A中产生的NO、NO2转化为HNO3,提高HNO3的利用率。答案为:安全瓶;提高HNO3的利用率;
(3)从反应C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O中N元素分析,生成3molH2C2O4,同时生成(9molNO2+3molNO),N元素共得电子(9×1+3×3)mol;则每生成1 mol H2C2O4转移电子的物质的量为6mol。答案为:6mol;
(4)从粗草酸晶体提纯H2C2O4·2H2O的方法是加水溶解后,再让草酸结晶析出。答案为:重结晶;
(5)①向Na2CO3溶液中滴加H2C2O4溶液,产生大量气体,应为CO2,反应满足强酸制弱酸的原则,从而说明草酸的酸性比碳酸。答案为:强;
②向NaClO溶液中加入过量H2C2O4溶液,有气泡产生,则生成CO2,ClO-被还原为Cl-,发生反应的离子方程式为:ClO-+H2C2O4= Cl-+2CO2↑+H2O。答案为:ClO-+H2C2O4= Cl-+2CO2↑+H2O。

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案