题目内容
7.某元素的离子带2个单位正电荷,它的核外电子排布为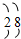 ,此元素在周期表中的位置是( )
,此元素在周期表中的位置是( )| A. | 第二周期零族 | B. | 第三周期ⅡA族 | C. | 第二周期ⅥA族 | D. | 第三周期IIIA |
分析 电子层数=周期数,最外层电子数=族序数,阳离子的核外电子数=原子序数-|所带电荷数|,原子核外电子排布为2、8、2,来确定原子序数、最外层电子数,进而确定族序数.
解答 解:电子层数=周期数,最外层电子数=族序数,阳离子的核外电子数=原子序数-|所带电荷数|,原子核外电子排布为2、8、2,所以是第三周期ⅡA族的元素,故选B.
点评 本题考查元素周期表及应用,为高频考点,把握原子结构与元素位置的关系为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
17.下列事实不能用勒夏特列原理解释的是( )
| A. | 适当加热新制的氯水时,溶液的pH逐渐减小 | |
| B. | 加催化剂,使N2和H2在一定条件下转化为NH3 | |
| C. | 可用浓氨水和氢氧化钠固体快速制取氨气 | |
| D. | 增大压强,有利于SO2与O2反应生成SO3 |
18.向一定量的Fe、FeO、Fe2O3的混合物中加入100mL浓度为1.0mol•L-1的盐酸,恰好使混合物完全溶解,放出224mL的气体(标准状况),所得溶液中加入KSCN溶液后无血红色出现.若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是( )
| A. | 11.2 g | B. | 5.6 g | C. | 2.8 g | D. | 1.4 g |
2.下列说法中,正确的是( )
| A. | 第ⅠA族元素都是金属元素 | |
| B. | 第ⅣA族非金属元素的单质只能形成原子晶体 | |
| C. | 第ⅥA族元素形成的单质,常温下有气、液、固三种状态 | |
| D. | 元素性质呈现周期性变化的根本原因是元素原子最外层电子数呈现周期性变化 |
12.已知:
①CaO(s)+H2O(1)═Ca(OH)2(aq);△H1
②CaO(s)+2HCl(g)═CaCl2(s)+H2O(1);△H2
③NH3(g)+HCl(g)═NH4Cl(s);△H3
④Ca(OH)2(aq)+2NH4Cl(s)═CaCl2(aq)+2NH3(g)+2H2O(1);△H4>0
下列关于上述反应焓变的判断正确的是( )
①CaO(s)+H2O(1)═Ca(OH)2(aq);△H1
②CaO(s)+2HCl(g)═CaCl2(s)+H2O(1);△H2
③NH3(g)+HCl(g)═NH4Cl(s);△H3
④Ca(OH)2(aq)+2NH4Cl(s)═CaCl2(aq)+2NH3(g)+2H2O(1);△H4>0
下列关于上述反应焓变的判断正确的是( )
| A. | △H1>0 | B. | △H4=△H1-△H2-2△H3 | ||
| C. | △H4=△H2-△H1-2△H3 | D. | △H4-△H1-△H2<0 |
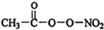 (PAN)等二次污染物.
(PAN)等二次污染物.
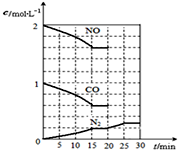 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.