题目内容
向某FeBr2溶液中,通入1.12L(标准状况下)的Cl2,测得溶液中c(Br-)=3c
(Cl-)=0.3mol/L。反应过程中溶液的体积变化忽略不计,则下列说法中正确的是
| A.原溶液的浓度约为0.13mol/L | B.反应后溶液中c(Fe3+)=0.1mol/L |
| C.反应后溶液中c(Fe3+)=c(Fe2+) | D.原溶液中c(Br-)= 0.4mol/L |
B
解析试题分析:由题意知氯气的物质的量是0.5mol,溶液中仍存在溴离子说明氯气不足,所以溶液中的c(Cl-)=0.1mol/L=1.12L/22.4L/mol×2/V,说明原溶液的体积是1L。若溶液中的阳离子只是Fe3+,根据电荷守恒可得c(Fe3+)=(0.3+0.1)/3mol/L,则原溶液中应存在n(Fe2+)=0.4/3mol,需要氯气的物质的量是0.4/3/2>0.5,与已知矛盾,所以溶液中还存在Fe2+。所以原溶液中FeBr2的浓度是0.15mol/L,n(Fe2+)=0.15mol,被0.5mol氯气氧化得Fe3+0.1mol,所以反应后溶液中c(Fe3+)=0.1mol/L,还余0.05mol/L Fe2+。则答案选B。
考点:考查氧化还原反应的计算,电荷守恒规律的应用

用Pt电极电解含有Cu2+和X3+各0.1 mol 的溶液,阴极析出固体物质的质量m g与溶液中通过电子的物质的量n mol的关系如图。则离子的氧化能力由大到小排列正确的是( )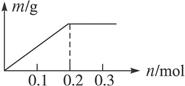
| A.Cu2+>X3+>H+ | B.H+>X3+>Cu2+ |
| C.Cu2+>H+>X3+ | D.X3+>H+>Cu2+ |
根据下列反应事实:①X+Y2+=X2++Y;②Z+2H2O(冷)=Z(OH)2+H2↑;
③Z2+氧化性比X2+弱;④由Y、W电极组成的电池,电极反应为W2++2e-=W、
Y-2e-=Y2+,可知X、Y、Z、W的还原性由强到弱的顺序为
| A.X>Z>Y>W | B.Z>W>X>Y | C.Z>Y>X>W | D.Z>X>Y>W |
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与3.36 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
| A.120mL | B.60 mL | C.40 mL | D.30 mL |
已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O,其中1mol氧化剂在反应中得到的电子为
| A.10mol | B.11mol | C.12mol | D.13mol |
下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向某溶液中加入盐酸酸化的BaCl2溶液 | 生成白色沉淀 | 该溶液中一定含有SO42— |
| B | 将少量的溴水滴入FeCl2、NaI的混合溶液中,再滴加CCl4,振荡、静置,向上层溶液中滴加KSCN溶液。再向上层溶液中滴加溴水 | 实验现象1: 上层溶液不变红, 下层溶液紫红色 实验现象2: 上层溶液变红 | 氧化性:Br2>Fe3+>I2 |
| C | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| D | 将一片铝箔置于酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面有致密Al2O3薄膜,且Al2O3熔点高于Al |