题目内容
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与3.36 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
| A.120mL | B.60 mL | C.40 mL | D.30 mL |
A
解析试题分析:足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与3.36L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,则Cu失去电子数等于氧气得到电子数,n(O2)=3.36L÷22.4L/mol=0.15mol,n(Cu)=0.15mol×4÷2=0.3mol,向所得硝酸铜溶液中加入5mol/L NaOH溶液至Cu2+恰好完全沉淀,由Cu~Cu(NO3)2~2NaOH可知,n(NaOH)=0.6mol,所有c(NaOH)=0.6mol÷5mol/L=0.12L=120mL,故A项正确。
考点:本题考查氧化还原反应的计算。

二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
(1)工业上制备ClO2的反应原理常采用:2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
① 浓盐酸在反应中显示出来的性质是_______(填序号)。
| A.只有还原性 | B.还原性和酸性 | C.只有氧化性 | D.氧化性和酸性 |
(2)目前已开发出用电解法制取ClO2的新工艺。
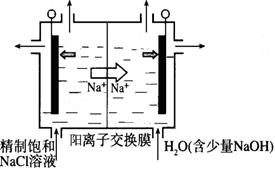
①上图示意用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。写出阳极产生ClO2的电极反应式:__________。
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为_________mol;用平衡移动原理解释阴极区pH增大的原因______________。
(3)ClO2对污水中Fe2+、Mn2+、S2—和CN-等有明显的去除效果。某工厂污水中含CN- a mg/L,现用ClO2将CN-氧化,只生成两种气体,其离子反应方程式为_______;处理100 m3这种污水,至少需要ClO2 _______ mol 。
某元素在化学反应中由化合态变为游离态,则该元素
| A.一定被氧化了 | B.一定被还原了 |
| C.既可能被还原也可能被氧化 | D.既不可能被氧化又不可能被还原 |
向某FeBr2溶液中,通入1.12L(标准状况下)的Cl2,测得溶液中c(Br-)=3c
(Cl-)=0.3mol/L。反应过程中溶液的体积变化忽略不计,则下列说法中正确的是
| A.原溶液的浓度约为0.13mol/L | B.反应后溶液中c(Fe3+)=0.1mol/L |
| C.反应后溶液中c(Fe3+)=c(Fe2+) | D.原溶液中c(Br-)= 0.4mol/L |
下列过程中没有发生氧化还原反应的是
| A.天然气燃烧提供热量 |
| B.氯水使红色纸张褪色 |
| C.钢铁制品在空气中被腐蚀 |
| D.二氧化硫通人品红溶液中,溶液褪色 |
“绿色化学”追求化工生产对环境零污染,下列物质中可以称为“绿色氧化剂”的是
| A.浓硫酸 | B.氯气 | C.双氧水 | D.漂白粉 |
下列反应既属于氧化还原反应,又是吸热反应的是( )
| A.铝与稀盐酸的反应 | B.灼热的木炭与CO2反应 |
| C.甲烷在氧气中的燃烧反应 | D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应 |
1.52 g铜镁合金完全溶解于50 mL密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况)。向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是
| A.该合金中铜与镁的物质的量之比是2?1 |
| B.该浓硝酸中HNO3的物质的量浓度是14.0 mol/L |
| C.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL |
| D.NO2和N2O4的混合气体中,NO2的体积分数是80% |