题目内容
【题目】下列图示与对应的叙述不相符的是
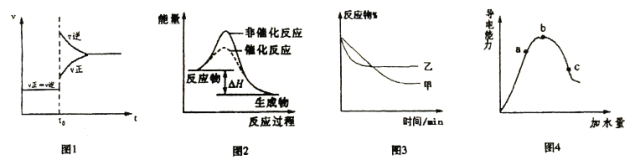
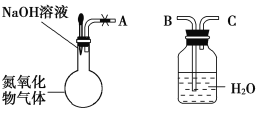
A.图1表示A(g)+B(g)![]() 3C(g)+2D(s) △H<0,达到平衡后升高温度成增大压强时的速率—时间变化图像
3C(g)+2D(s) △H<0,达到平衡后升高温度成增大压强时的速率—时间变化图像
B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图3表示压强对可逆反应A(g)+B(g)![]() 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
D.图4表示冰醋酸加水稀释,导电能力的变化图像,其中b点醋酸电高程度最大
【答案】D
【解析】
A. 图1表示A(g)+B(g)![]() 3C(g)+2D(s) △H<0,达到平衡后,升高温度,正逆反应速率都增大,由于温度升高,化学平衡向着吸热的方向移动,故逆向移动,增大压强,平衡向着体积减小的方向移动,即逆向移动,故A图象复合,故A正确;
3C(g)+2D(s) △H<0,达到平衡后,升高温度,正逆反应速率都增大,由于温度升高,化学平衡向着吸热的方向移动,故逆向移动,增大压强,平衡向着体积减小的方向移动,即逆向移动,故A图象复合,故A正确;
B. 反应物的总能量大于生成物的总能量,则反应是放热反应,加入催化剂会降低活化能,改变反应的速率,但反应热不改变,故B正确;
C. 乙的压强比甲的压强大,则增大压强,平衡逆向移动,则反应物的浓度比较大,则图象符合题意,故C正确;
D. b点表示醋酸的导电能力最强,对于弱电解质,溶液越稀,电离程度越大,c点表示醋酸电高程度最大,故D错误;
答案选D。

【题目】一定温度下,在3个1.0 L的恒容密闭容器中分别进行反应2X(g)+Y(g)![]() Z(g) ΔH,达到平衡。相关数据如下表。
Z(g) ΔH,达到平衡。相关数据如下表。
容器 | 温度/K | 物质的起始浓度/ mol·L-1 | 物质的平衡浓度/ mol·L-1 | ||
c(X) | c(Y) | c(Z) | c(Z) | ||
I | 400 | 0.20 | 0.10 | 0 | 0.080 |
II | 400 | 0.40 | 0.20 | 0 | a |
III | 500 | 0.20 | 0.10 | 0 | 0.025 |
下列说法不正确的是
A. 平衡时,X的转化率:II>I
B. 平衡常数:K(II)>K(I)
C. 达到平衡所需时间:III<I
D. 反应的ΔH<0
【题目】探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L1 H2C2O4的pH=1.3)
实验 | 装置 | 试剂a | 现象 |
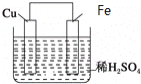
① |
| Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
② | 少量NaHCO3溶液 | 产生气泡 | |
③ | 酸性KMnO4溶液 | 紫色溶液褪色 | |
④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
A. H2C2O4有酸性,Ca(OH)2+ H2C2O4![]() CaC2O4↓+2H2O
CaC2O4↓+2H2O
B. 酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4![]() NaHC2O4+CO2↑+H2O
NaHC2O4+CO2↑+H2O
C. H2C2O4具有还原性,2![]() +5
+5![]() +16H+
+16H+![]() 2Mn2++10CO2↑+ 8H2O
2Mn2++10CO2↑+ 8H2O
D. H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH![]() C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O