题目内容
20.在①甲烷;②苯;③聚乙烯;④乙醛;⑤2-丁炔;⑥环己烷;⑦邻二甲苯;⑧环己烯这8种物质种中,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )| A. | ③⑤⑧ | B. | ④⑤⑦ | C. | ④⑤⑧ | D. | ③⑥⑦ |
分析 8种物质都属于烃,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的有机物一般应具有还原性,往往应含有不饱和键,以此解答该题.
解答 解:①甲烷为饱和烃,不能与酸性高锰酸钾溶液和溴水反应,故①错误;
②苯不能与酸性高锰酸钾溶液和溴水反应,故②错误;
③聚乙烯不含不饱和键,不能与酸性高锰酸钾溶液和溴水反应,故③错误;
④乙醛含有醛基,可被酸性高锰酸钾或溴水氧化,故④正确;
⑤2-丁炔含有不饱和键,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,故⑤正确;
⑥环己烷不含不饱和键,不能与酸性高锰酸钾溶液和溴水反应,故⑥错误;
⑦邻二甲苯只能与酸性高锰酸钾发生反应,但不能与溴水反应,故⑦错误;
⑧环己烯含有不饱和键,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,故⑧正确.
故选C.
点评 本题考查有机物的结构和性质,为高频考点,题目难度不大,注意把握有机物官能团或基团的性质,性质官能团的性质解答该题.

练习册系列答案
相关题目
10.已知:将C12通入适量NaOH溶液,产物中可能有NaCl、NaClO、NaClO3,且$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$的值仅与温度高低有关.当n(NaOH)=6amol时,下列有关说法正确的是( )
| A. | 改变温度,反应中转移电子的物质的量n的范围:3amol≤n≤5amol | |
| B. | 改变温度,产物中NaCl的最小理论产量为4amol | |
| C. | 参加反应的氯气的物质的量3amol | |
| D. | 某温度下,若反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=6,则溶液中$\frac{c(C{l}^{-})}{c(C{O}_{3}^{-})}=\frac{1}{2}$ |
11.下列括号中对日常生活的变化判断正确的是( )
| A. | 嘴嚼米饭时有甜味(化学变化) | |
| B. | 玻璃窗破裂(化学变化) | |
| C. | 二氧化碳使澄清的石灰水变浑浊(物理变化) | |
| D. | 纯净物加热后变为混合物(物理变化) |
15.下列混合物应选用蒸馏操作法分离的是( )
| A. | 硝酸钾和氯化钠的混合物 | B. | 溴水 | ||
| C. | 汽油和柴油 | D. | 四氯化碳和水 |
12.反应N2+3H2?2NH3,开始时N2的浓度为3mol•L-1,H2的浓度为5mol•L-1,3min后测得NH3浓度为0.6mol•L-1,则此时间内,下列反应速率表示正确的是( )
| A. | v(NH3)=0.2 mol•L-1•s-1 | B. | v(N2)=1.0 mol•L-1•min-1 | ||
| C. | v(H2)=1.67 mol•L-1•min-1 | D. | v(H2)=0.3 mol•L-1•min-1 |
9.在检验溶液中SO42-的过程中,下列操作中正确的是( )
| A. | 先加入稀硝酸,无沉淀产生,然后再加硝酸钡溶液,产生白色沉淀,证明有SO42-存在 | |
| B. | 先加入硝酸钡溶液,产生白色沉淀,然后再加稀硝酸,沉淀不溶解,证明有SO42-存在 | |
| C. | 先加入稀盐酸,无产生沉淀,然后再加氯化钡溶液,产生白色沉淀,证明有SO42-存在 | |
| D. | 先加入氯化钡溶液,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有SO42-存在 |
 .
.
 ,由两种元素组成的三原子共价化合物的电子式
,由两种元素组成的三原子共价化合物的电子式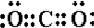 或
或 .(各写1种)
.(各写1种)