题目内容
10.有H、C、O、Cl、Na五种元素.(1)由两种元素组成的四原子离子化合物的电子式
 ,由两种元素组成的三原子共价化合物的电子式
,由两种元素组成的三原子共价化合物的电子式 或
或 .(各写1种)
.(各写1种)(2)在由三种元素组成的化合物里,其中离子化合物的化学式Na2CO3、NaClO,共价化合物的化学式H2CO3、HClO.(组成元素不能完全相同)(各写2种)
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,金属氧化物、大多数盐及铵盐中都含有离子键,第IA族(H元素除外)、第IIA族元素和第VIA族、第VIIA族元素之间易形成离子键,含有离子键的化合物为离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物.
(1)钠为活泼金属,与非金属可形成离子化合物,非金属元素之间可形成共价化合物;离子化合物,其电子式由阴、阳离子的电子式组合而成,相同的离子不能合并;共价化合物,其电子式由对应原子的电子式组成,并要表示出两原子之间的共用电子对情况;
(2)由三种元素组成的化合物,离子化合物中一定含Na元素,共价化合物中一定不含钠元素.
解答 解:(1)活泼金属元素和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,所以在由两种元素组成的化合物里,属于离子化合物的有Na2O、NaCl、Na2O2,四原子离子化合物为Na2O2,是钠离子和过氧根离子构成的离子化合物,钠离子失电子形成阳离子,过氧根离子得到电子形成阴离子,电子式为 ,
,
属于共价化合物的有CO2、CO、CH4、H2O,三原子共价化合物为CO2、H2O,CO2是共价化合物,碳原子有四个电子分别和氧原子形成两对共用电子对,电子式为 ,H2O是共价化合物,是由原子和氢原子形成共价键,电子式为
,H2O是共价化合物,是由原子和氢原子形成共价键,电子式为 ,
,
故答案为: ;
; 或
或 ;
;
(2)在由三种元素组成的化合物里,其中离子化合物有Na2CO3、NaClO,属于共价化合物的有H2CO3、HClO,
故答案为:Na2CO3、NaClO;H2CO3、HClO.
点评 本题考查离子化合物和共价化合物的判断,侧重考查学生对概念的理解,明确化合物和化学键的关系是解本题关键,注意答案不唯一,注意掌握电子式的书写方法,题目难度不大.

| A. | ③⑤⑧ | B. | ④⑤⑦ | C. | ④⑤⑧ | D. | ③⑥⑦ |
| A. | 用A表示的反应速率是0.4mol•(L•min)-1 | |
| B. | 在2min末的反应速率,用B表示是0.3mol•(L•min)-1 | |
| C. | 分别用B、C、D表示反应的速率,其比是3:2:1 | |
| D. | 在这2min内用B和C表示的反应速率的值都是逐渐减小的 |
| A. | ${\;}_{a}^{b}$R | B. | ${\;}_{a-2}^{a+b-2}$R | C. | ${\;}_{a+2}^{a+b+2}$R | D. | ${\;}_{a-2}^{a+b}$R |
| 实 验 步 骤 | 解 释 或 实 验 结 论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空: (1)A的相对分子质量为:90. |
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g. | (2)A的分子式为:C3H6O3. |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况). | (3)用结构简式表示A中含有的官能团: -COOH、-OH. |
(4)A的核磁共振氢谱如下图: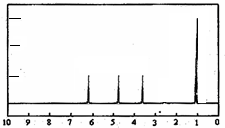 | (4)A中含有4种氢原子. |
(5)综上所述,A的结构简式  . . | |
| A. | 甲烷和乙烷 | B. | 正丁烷和异丁烷 | C. | 金刚石和石墨 | D. | 35Cl 和37Cl |
| A. | 直接分液 | |
| B. | 加入氢氧化钠溶液后,充分振荡,静置后分液 | |
| C. | 直接蒸馏 | |
| D. | 加入过量溴水,过滤 |
(1)请完成SO2与过量NaOH溶液反应的化学方程式:SO2+2NaOH=Na2SO3+H2O.
(2)反应Cl2+Na2SO3+2NaOH═2NaCl+Na2SO4+H2O中的氧化剂为Cl2.
(3)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响).
①提出合理假设.
假设1:只存在SO32-;
假设2:只存在ClO-;
假设3:既不存在SO32-也不存在ClO-
②基于假设3(即验证假设3成立),设计实验方案,进行实验.请在答题卡上写出实验步骤以及预期现象和结论.限选实验试剂:3mol.L-1H2SO4、1mom.L-1NaOH、0.01mol.L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管中,滴加3mol.L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中 | |
| 步骤2:向A试管中滴加1-2滴0.01mol.L-1KMnO4溶液. | 溶液呈浅紫色,则证明不存在SO32-, 则证明不存在SO32-. |
| 步骤3:向B试管中滴加1-2滴淀粉-KI溶液. | 溶液不变蓝色, 则证明不存在ClO-. |