题目内容
8.用分液漏斗可以分离的一组混合物是( )| A. | 溴苯和水 | B. | 丙醇和乙二醇 | C. | 碘和乙醇 | D. | 甘油和水 |
分析 分液漏斗可以将互不相溶的两层液体分开,溴苯和水不互溶,醇和醇互溶,碘单质易溶于醇,甘油和水互溶.
解答 解:A.溴苯和水是互不相溶的两层液体,溴苯在下层,能用分液漏斗分离,故A正确;
B.丙醇和乙二醇是互溶的两种醇,不能用分液漏斗分离,故B错误;
C.碘和乙醇是互溶的,不能用分液漏斗分离,故C错误;
D.甘油是丙三醇,和水是互溶的,不能用分液漏斗分离,故D错误;
故选A.
点评 本题考查学生物质分离方法中的分液法,掌握分液的条件、物质的溶解性是解题的关键,题目难度不大.

练习册系列答案
相关题目
3.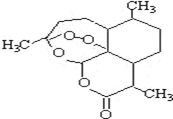 被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.截至2005年底,已被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )
被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.截至2005年底,已被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )
 被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.截至2005年底,已被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )
被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.截至2005年底,已被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )| A. | 分子式为:C16H22O5 | |
| B. | 该化合物在一定条件下不能与NaOH溶液反应 | |
| C. | 该化合物中含有过氧键,一定条件下有氧化性 | |
| D. | 青蒿素易溶于水 |
4.X、Y、Z、W、M、N六种元素均位于元素周期表的前四周期(如图所示).有关这六种元素的下列叙述中不正确的是( )


| A. | 元素的简单离子半径M<W<Z | |
| B. | Y元素在自然界存在多种同素异形体 | |
| C. | 最高价氧化物的水化物酸性W>N | |
| D. | N与Z的质子数之差为16 |
1.在低温下电解饱和KHSO4溶液可制备K2S2O8,电解装置如图所示.下列说法不正确的是( )

| A. | 阳极的电极反应式为2SO42--2e-═S2O82- | |
| B. | 电解的总反应方程式为2KHSO4$\frac{\underline{\;通电\;}}{\;}$K2S2O8+H2↑ | |
| C. | 一段时间后,溶液的pH减小 | |
| D. | 电解过程中,阳极产生微量能使湿润的淀粉KI试纸变蓝的有色单质气体,该气体可能是O3 |
3.现有如下说法:
①在离子化合物里,只存在离子键,没有共价键.
②金属和非金属只能化合形成离子键.
③离子键是阳离子、阴离子的相互吸引.
④在PCl5、CCl4中各原子最外层均能达到8电子的稳定结构.
⑤共价键只存在于共价化合物中.
上述各种说法正确的是( )
①在离子化合物里,只存在离子键,没有共价键.
②金属和非金属只能化合形成离子键.
③离子键是阳离子、阴离子的相互吸引.
④在PCl5、CCl4中各原子最外层均能达到8电子的稳定结构.
⑤共价键只存在于共价化合物中.
上述各种说法正确的是( )
| A. | ①②⑤正确 | B. | 都不正确 | ||
| C. | ④正确,其他不正确 | D. | 仅①不正确 |
13.NH4Cl晶体中含有多种化学键,其中一定不含有的化学键是( )
| A. | 离子键 | B. | π键 | C. | 配位键 | D. | 氢键 |
17.下列电子式书写错误的是( )
| A. | 甲基: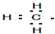 | B. | CaC2: | C. | NH4+: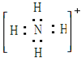 | D. | 氯仿: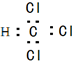 |
18.下列分子中所有原子均满足最外层8电子结构的是( )
| A. | SF6 | B. | BeCl2 | C. | CO2 | D. | PCl5 |
 .
.