题目内容
4.X、Y、Z、W、M、N六种元素均位于元素周期表的前四周期(如图所示).有关这六种元素的下列叙述中不正确的是( )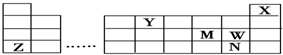
| A. | 元素的简单离子半径M<W<Z | |
| B. | Y元素在自然界存在多种同素异形体 | |
| C. | 最高价氧化物的水化物酸性W>N | |
| D. | N与Z的质子数之差为16 |
分析 由元素在周期表中的位置可知X、Y、Z、W、M、N分别为He、C、K、Cl、S、Br等元素,
A.核外电子排布相同的离子,核电荷数越大离子半径越小;
B.Y为C元素,存在金刚石、石墨等同素异形体;
C.元素的非金属性越强,对应的最高价氧化物的水化物酸性越强;
D.Z的质子数为19,N的质子数为35.
解答 解:由元素在周期表中的位置可知X、Y、Z、W、M、N分别为He、C、K、Cl、S、Br等元素,
A.Z、W、M对应的离子具有核外电子排布相同的离子,核电荷数越大离子半径越小,故A错误;
B.Y为C元素,存在金刚石、石墨等同素异形体,故B正确;
C.非金属性W>N,元素的非金属性越强,对应的最高价氧化物的水化物酸性越强,故C正确;
D.Z的质子数为19,N的质子数为35,质子数之差为16,故D正确.
故选A.
点评 本题考查了元素周期表和元素周期律的综合应用,为高频考点,根据元素周期律中电负性大小、原子结构、非金属性强弱等规律来分析解答,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
15.分别燃烧等物质的量的下列各组物质,其中消耗氧气量相等的是( )
①C2H2 与CH3CHO
②C2H2与C6H6
③C7H8与C6H12
④HCOOCH3与CH3COOH.
①C2H2 与CH3CHO
②C2H2与C6H6
③C7H8与C6H12
④HCOOCH3与CH3COOH.
| A. | ①③④ | B. | ①②③④ | C. | ①④ | D. | ②④ |
16.下面是某研究小组研究的关于不同催化剂对H2O2 分解反应的催化效率.
(1)写出H2O2 在催化剂作用下分解反应的化学方程式2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
(2)从上表可以得出:活性炭、FeCl3、KI 和MnO2(粉末状)几种催化剂中,催化效率由大到小的顺序是MnO2(粉末状)>FeCl3>KI>活性炭,等质量的固体催化剂,颗粒大小对催化效率有什么影响颗粒越小催化效果越好.
(3)实验发现新鲜的动物肝脏对H2O2 的分解也有显著的催化作用,但当往溶液中加入盐酸,或给溶液加热时,就会失去催化能力,合理的解释是催化剂失去活性.
| 催化剂(0.1g) | 活性炭 | FeCl3 | KI | MnO2颗粒状 | MnO2粉末状 |
| 前15s产生氧气的量(ml)[来 | 5 | 11 | 7 | 8[ | 11 |
| 前30s产生氧气的量(ml) | 8 | 16 | 11 | 11 | 21 |
| 前45s产生氧气的量(ml) | 11 | 20 | 15 | 18 | 35 |
| 前60s产生氧气的量(ml) | 15 | 24 | 20 | 26 | 49 |
(2)从上表可以得出:活性炭、FeCl3、KI 和MnO2(粉末状)几种催化剂中,催化效率由大到小的顺序是MnO2(粉末状)>FeCl3>KI>活性炭,等质量的固体催化剂,颗粒大小对催化效率有什么影响颗粒越小催化效果越好.
(3)实验发现新鲜的动物肝脏对H2O2 的分解也有显著的催化作用,但当往溶液中加入盐酸,或给溶液加热时,就会失去催化能力,合理的解释是催化剂失去活性.
8.用分液漏斗可以分离的一组混合物是( )
| A. | 溴苯和水 | B. | 丙醇和乙二醇 | C. | 碘和乙醇 | D. | 甘油和水 |
9.元素性质呈周期性变化的决定因素是( )
| A. | 元素原子半径大小呈周期性变化 | |
| B. | 元素原子量依次递增 | |
| C. | 元素的最高正化合价呈周期性变化 | |
| D. | 元素原子最外层电子排布呈周期性变化 |
 .
. .
.