题目内容
3.现有如下说法:①在离子化合物里,只存在离子键,没有共价键.
②金属和非金属只能化合形成离子键.
③离子键是阳离子、阴离子的相互吸引.
④在PCl5、CCl4中各原子最外层均能达到8电子的稳定结构.
⑤共价键只存在于共价化合物中.
上述各种说法正确的是( )
| A. | ①②⑤正确 | B. | 都不正确 | ||
| C. | ④正确,其他不正确 | D. | 仅①不正确 |
分析 ①在离子化合物里,一定含有离子键,可能含有共价键;
②金属和非金属元素可能形成共价键;
③离子键是阳离子、阴离子的相互作用;
④在分子中,中心原子价电子数+化合价的绝对值=8时,该分子中各原子达到8电子稳定结构,但氢化物除外;
⑤共价键存在于共价化合物或多原子分子的单质中.
解答 解:①在离子化合物里,一定含有离子键,可能含有共价键,如KOH,故错误;
②金属和非金属元素可能形成共价键,如氯化铝,故错误;
③离子键是阳离子、阴离子的相互作用,相互作用包含吸引力和排斥力,故错误;
④在分子中,中心原子价电子数+化合价的绝对值=8时,该分子中各原子达到8电子稳定结构,但氢化物除外,五氯化磷中P原子价电子数+化合价的绝对值=5=10,所以该分子中P原子不是8电子稳定结构,故错误;
⑤共价键存在于共价化合物或多原子分子的单质中,如氧气、臭氧等,故错误;
故选B.
点评 本题考查化学键,侧重考查基本概念,明确离子键和共价键的区别是解本题关键,会判断8电子稳定结构,题目难度不大.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
18.A、B、C三种元素的核电荷数依次为a、b、c,它们的离子An+、Bn-、Cm-具有相同的电子层结构,且n>m,则下列关系正确的是( )
| A. | a>b>c | B. | a>c>b | C. | a=b+m+n | D. | a=c+n+m |
16.下面是某研究小组研究的关于不同催化剂对H2O2 分解反应的催化效率.
(1)写出H2O2 在催化剂作用下分解反应的化学方程式2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
(2)从上表可以得出:活性炭、FeCl3、KI 和MnO2(粉末状)几种催化剂中,催化效率由大到小的顺序是MnO2(粉末状)>FeCl3>KI>活性炭,等质量的固体催化剂,颗粒大小对催化效率有什么影响颗粒越小催化效果越好.
(3)实验发现新鲜的动物肝脏对H2O2 的分解也有显著的催化作用,但当往溶液中加入盐酸,或给溶液加热时,就会失去催化能力,合理的解释是催化剂失去活性.
| 催化剂(0.1g) | 活性炭 | FeCl3 | KI | MnO2颗粒状 | MnO2粉末状 |
| 前15s产生氧气的量(ml)[来 | 5 | 11 | 7 | 8[ | 11 |
| 前30s产生氧气的量(ml) | 8 | 16 | 11 | 11 | 21 |
| 前45s产生氧气的量(ml) | 11 | 20 | 15 | 18 | 35 |
| 前60s产生氧气的量(ml) | 15 | 24 | 20 | 26 | 49 |
(2)从上表可以得出:活性炭、FeCl3、KI 和MnO2(粉末状)几种催化剂中,催化效率由大到小的顺序是MnO2(粉末状)>FeCl3>KI>活性炭,等质量的固体催化剂,颗粒大小对催化效率有什么影响颗粒越小催化效果越好.
(3)实验发现新鲜的动物肝脏对H2O2 的分解也有显著的催化作用,但当往溶液中加入盐酸,或给溶液加热时,就会失去催化能力,合理的解释是催化剂失去活性.
3. 现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题
现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题
(1)B基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形.
(2)C和与其左右相邻元素原子的第一电离能由大到小的顺序是Mg>Al>Na.
(3)①DE3中心原子的杂化方式为sp3杂化,该分子中的键角比离子DE4+中的键角小的原因是孤电子对与成键电子对的排斥作用力大于成键电子对之间的排斥作用力
②将E的单质通入到黄血盐{K4[Fe(CN)6]}溶液中,可得到赤血盐{K3[Fe(CN)6]}.该反应的离子方程式为2[Fe(CN)6]4-+Cl2=2[Fe(CN)6]3-+2Cl-
③已知含E的一种化合物与过氧化氢发生如下反应(已配平):H2O2+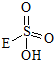 →
→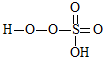 +HE,请写出横线上物质的结构式.
+HE,请写出横线上物质的结构式.
(4)F位于d区,价电子排布式为3d54s1.
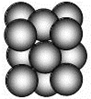
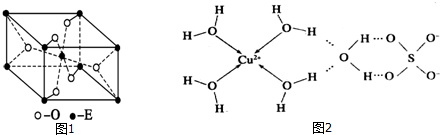
(5)G单质晶体中原子的堆积方式为面心立方最密堆积(如图),则晶胞中每个原子的配位数为12.假设晶胞边长为a,原子半径为r,列式表示该晶胞的空间利用率为$\frac{\sqrt{2}}{6}π$.
 现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题
现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F 是前四周期原子电子轨道表示式中单电子数最多的元素 |
| G在周期表的第十一列 |
(2)C和与其左右相邻元素原子的第一电离能由大到小的顺序是Mg>Al>Na.
(3)①DE3中心原子的杂化方式为sp3杂化,该分子中的键角比离子DE4+中的键角小的原因是孤电子对与成键电子对的排斥作用力大于成键电子对之间的排斥作用力
②将E的单质通入到黄血盐{K4[Fe(CN)6]}溶液中,可得到赤血盐{K3[Fe(CN)6]}.该反应的离子方程式为2[Fe(CN)6]4-+Cl2=2[Fe(CN)6]3-+2Cl-
③已知含E的一种化合物与过氧化氢发生如下反应(已配平):H2O2+
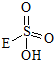 →
→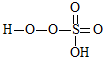 +HE,请写出横线上物质的结构式.
+HE,请写出横线上物质的结构式.(4)F位于d区,价电子排布式为3d54s1.
(5)G单质晶体中原子的堆积方式为面心立方最密堆积(如图),则晶胞中每个原子的配位数为12.假设晶胞边长为a,原子半径为r,列式表示该晶胞的空间利用率为$\frac{\sqrt{2}}{6}π$.
8.用分液漏斗可以分离的一组混合物是( )
| A. | 溴苯和水 | B. | 丙醇和乙二醇 | C. | 碘和乙醇 | D. | 甘油和水 |
13.少量铁粉与100mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率可以使用如下方法( )
| A. | 加H2O | B. | 滴入几滴浓盐酸 | ||
| C. | 增大压强 | D. | 升高温度(不考虑盐酸挥发) |
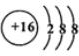 ;
;