题目内容
【题目】新能源汽车的核心部 件是锂离子电池,磷酸亚铁锂(LiFePO4)以其高倍率性、高比能量、高循环特征、高安全性、低成本、环保等优点而逐渐成为“能源新宠”。
[方法一]高温固相法是磷酸亚铁锂生产的主要方法。通常以亚铁盐(如FeC2O42H2O)磷酸盐和锂盐为原料,充分混匀后,在惰性气氛的保护气中先经过较低温预分解,再经过高温焙烧,研磨粉碎制成。其反应原理如下:
Li2CO3+2FeC2O42H2O+2NH4H2PO4 =2NH3↑+3CO2↑+ + +
(1)完成上述化学方程式______。
(2)理论上,反应中每转移0.15mol电子,会生成 ______gLiFePO4。
[方法二]以铁红、锂辉石LiAl(SiO3)2(含少量Ca2+、Mg2+的盐)、碳粉等原料来生产磷酸亚铁锂。其主要工艺流程如图:
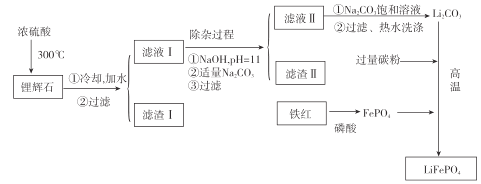
已知:2LiAl(SiO3)2+H2SO4(浓)![]() Li2SO4 + Al2O34SiO2H2O↓
Li2SO4 + Al2O34SiO2H2O↓
温度/℃ | 20 | 40 | 60 | 80 |
溶解度(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
溶解度(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.5 |
(1)向滤液II中加入饱和Na2CO3溶液,过滤后 ,用“热水洗涤”的原因是_____。
(2)滤渣II的主要成分是_______(填化学式)。
(3)写出在高温下生成磷酸亚铁锂的化学方程式:_____________。
(4)工业上,将 Li2CO3粗品制备成高纯 Li2CO3 的部分工艺如下:
①将粗产品Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择半透膜隔开,用惰性电极电解,阳极的电极反应式是____________。
②电解后向产品LiOH 溶液中加入过量 NH4 HCO3并加热,过滤、烘干得高纯 Li2CO3。 请写出生成Li2CO3的化学方程式:___________。
【答案】2LiFePO4 2CO↑ 7H2O↑ 23.7 Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3 的损失 Mg(OH)2、CaCO3 2FePO4+Li2CO3+2C![]() 2LiFePO4+3CO↑ 2Cl--2e-=Cl2↑ 2LiOH+NH4HCO3
2LiFePO4+3CO↑ 2Cl--2e-=Cl2↑ 2LiOH+NH4HCO3![]() Li2CO3 ↓+2H2O+NH3 ↑
Li2CO3 ↓+2H2O+NH3 ↑
【解析】
[方法一](1)根据原子守恒分析;
(2)C2O42-中C的化合价为+3价,生成CO和CO2,C元素的化合价分别为+2价、+3价,根据电子与LiFePO4的关系计算;
[方法二]2LiAl(SiO3)2+H2SO4(浓)=Li2SO4+Al2O3·4SiO2·H2O↓,冷却加水过滤得到滤液I和滤渣I,滤渣中含有Al2O3·4SiO2·H2O↓,滤液中含有Li2SO4、MgSO4、CaSO4,向滤液中加入NaOH、Na2CO3,镁离子和NaOH反应生成氢氧化镁沉淀,钙离子和碳酸钠反应生成碳酸钙沉淀,所以滤渣II为Mg(OH)2、CaCO3,滤液中含有硫酸锂,向滤液中加入饱和碳酸钠得到碳酸锂沉淀,铁和磷酸反应生成磷酸铁,磷酸铁和碳酸锂在高温下反应生成LiFePO4;
[方法一](1)由原子守恒可知,Li2CO3+2FeC2O4·2H2O+2NH4H2PO4═2LiFePO4+2NH3↑+3CO2↑+2CO↑+7H2O↑,故答案为:2LiFePO4;2CO↑;7H2O↑;
(2)C2O42-中C的化合价为+3价,生成CO和CO2,C元素的化合价分别为+2价、+3价,生成2molCO转移2mol电子,同时生成2molLiFePO4,则当反应中每转移0.15mol电子,生成0.15molLiFePO4,其质量为23.7g,故答案为:23.7;
[方法二](1)向滤液II中加入饱和Na2CO3溶液,过滤后 ,用“热水洗涤”的原因是Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3 的损失。
故答案为:Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3 的损失;
(2)向滤液中加入NaOH、Na2CO3,镁离子和NaOH反应生成氢氧化镁沉淀,钙离子和碳酸钠反应生成碳酸钙沉淀,所以滤渣II为Mg(OH)2、CaCO3。故答案为:Mg(OH)2、CaCO3;
(3)在高温下FePO4被碳还原生成磷酸亚铁锂的化学方程式:2FePO4+Li2CO3+2C![]() 2LiFePO4+3CO↑ 。 故答案为:2FePO4+Li2CO3+2C
2LiFePO4+3CO↑ 。 故答案为:2FePO4+Li2CO3+2C![]() 2LiFePO4+3CO↑ ;
2LiFePO4+3CO↑ ;
(4)工业上,将 Li2CO3粗品制备成高纯 Li2CO3 的部分工艺如下:
①将粗产品Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择半透膜隔开,用惰性电极电解,阳极氯离子失电子被氧化,电极反应式是2Cl--2e-=Cl2↑ 。故答案为:2Cl--2e-=Cl2↑ ;
②电解后向产品LiOH 溶液中加入过量 NH4 HCO3并加热,过滤、烘干得高纯 Li2CO3。 生成Li2CO3的化学方程式:2LiOH+NH4HCO3![]() Li2CO3 ↓+2H2O+NH3 ↑。故答案为:2LiOH+NH4HCO3
Li2CO3 ↓+2H2O+NH3 ↑。故答案为:2LiOH+NH4HCO3![]() Li2CO3 ↓+2H2O+NH3 ↑。
Li2CO3 ↓+2H2O+NH3 ↑。