题目内容
13.如表为元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法错误的是( )| Q | R | ||
| T | W | ||
| A. | 气态氢化物稳定性:R>Q | |
| B. | 元素T的离子结构示意图为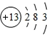 | |
| C. | 与W同主族的某元素形成的18电子的氢化物分子中既有极性键又有非极性键 | |
| D. | W可形成多种含氧酸 |
分析 根据短周期元素在周期表中的位置知,Q、R是第二周期元素,T、W是第三周期元素,四种元素只有一种是金属元素,四种元素中T的金属性最强,则只能是T为金属元素,Q、R、T、W有两种可能,分别为B、C、Mg、P,或C、N、Al、S,结合元素周期律解答.
解答 解:根据短周期元素在周期表中的位置知,Q、R是第二周期元素,T、W是第三周期元素,四种元素只有一种是金属元素,四种元素中T的金属性最强,则只能是T为金属元素,Q、R、T、W有两种可能,分别为B、C、Mg、P,或C、N、Al、S,
A.同一周期从左到右非金属性逐渐增强,其氢化物的稳定性逐渐增强,则气态氢化物稳定性:R>Q,故A正确;
B.T为Mg元素或Al元素,则其离子结构示意图为 或
或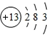 ,故B错误;
,故B错误;
C.W为P或S,与其同主族的元素N或O形成的18电子的氢化物分子为H2O2或N2H4,分子中既有极性键又有非极性键,故C正确;
D.W为P或S,可形成多种含氧酸,如磷酸、亚磷酸,硫酸、亚硫酸,故D正确;
故选B.
点评 本题侧重考查原子结构、元素周期表结构、元素周期律,难度不大,属于易错题目,注意把握元素周期表的结构.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
3.有机物在生活中的应用非常广泛.下列有关说法正确的是( )
| A. | 食用植物油均可水解生成氨基酸 | |
| B. | 铺路用的沥青主要含有C、H、O等元素 | |
| C. | 做衣服的棉、麻的主要成分是纤维素 | |
| D. | 煤经过汽化、液化等物理变化可转化为清洁燃料 |
4.下列对分子的性质的解释中,不正确的是( )
| A. | 水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键所致 | |
| B. | 乳酸(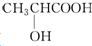 )有一对手性异构体,因为其分子中含有一个手性碳原子 )有一对手性异构体,因为其分子中含有一个手性碳原子 | |
| C. | 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 | |
| D. | 酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数比HClO的多 |
18.下列说法正确的是( )
| A. | 对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 | |
| B. | 乳酸薄荷醇酯(如图 )能发生水解、氧化、消去反应、以及与氢气的加成反应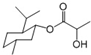 | |
| C. | 0.1mol丙烯酸中含有双键的数目为0.1NA | |
| D. | 乙醛和丙烯醛(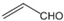 )不是同系物,它们与氢气充分反应后的产物是同系物 )不是同系物,它们与氢气充分反应后的产物是同系物 |
5.下列各组物质熔化或气化时,所克服的微粒间的作用力属同种类型的是( )
| A. | SiO2和CaO的熔化 | B. | 氧化钠和铁的熔化 | ||
| C. | 碘和干冰的气化 | D. | 晶体硅和晶体硫的熔化 |
2.下列说法不正确的是( )
| A. | 容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| B. | 在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、普通玻璃棒进行搅拌使酸和碱充分反应、准确读取实验时温度计最高温度、并且取2-3 次的实验平均值等措施,以达到良好的实验效果 | |
| C. | 金属着火时,可用细沙覆盖灭火;电器设备引起的火灾,不可用泡沫灭火器灭火 | |
| D. | 在4mL0.1mol•L-1的K2Cr2O7溶液中滴加数滴1mol•L-1的NaOH溶液,溶液颜色从橙色变成黄色 |
3.镁-次氯酸盐燃料电池,它具有比能量高、安全方便等优点.该电池的正极反应式为:ClO-+H2O+2e-=Cl-+2OH-,关于该电池的叙述正确的是( )
| A. | 该电池中镁为负极,发生还原反应 | |
| B. | 电池工作时,OH-向正极移动 | |
| C. | 该电池的总反应为:Mg+ClO-+H2O=Mg(OH)2↓+Cl- | |
| D. | 电池工作时,正极周围溶液的pH将不断变小 |
 、F
、F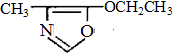 .
.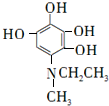 等.
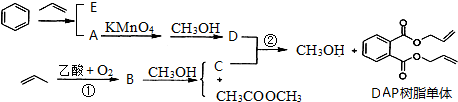
等. .
.

 .
. .
.