题目内容
8.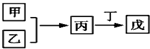 甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙均为单质,它们的转化关系如图所示(某些条件和部分产物已略去).下列说法不正确的是( )
甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙均为单质,它们的转化关系如图所示(某些条件和部分产物已略去).下列说法不正确的是( )| A. | 若甲既能与盐酸反应又能与NaOH溶液反应,则丙可能属于两性氧化物 | |
| B. | 若丙、丁混合产生白烟,且丙为18电子分子,则乙的水溶液可能具有漂白作用 | |
| C. | 若甲、丙、戊含有同一种元素,该元素的化合价由低到高的顺序可能为甲<丙<戊 | |
| D. | 若甲为短周期中原子半径最大的主族元素的单质,且戊为碱,则丙只能为Na2O2 |
分析 A.甲为单质,既能与盐酸反应又能与NaOH溶液反应,则甲为Al;
B.甲为短周期中原子半径最大的主族元素的单质,则甲为Na,乙为氧气;
C.丙、丁混合产生白烟,且丙为18电子分子,丁为10电子分子,则丙为HCl,丁为NH3;
D.若甲、丙、戊含有同一种元素,当甲为S,乙为氧气,丙为二氧化硫,戊为硫酸,则含S元素的化合价符合题意.
解答 解:A.甲为单质,既能与盐酸反应又能与NaOH溶液反应,则甲为Al,乙为氧气,二者反应生成丙为氧化铝,属于两性氧化物,故A正确;
B.丙、丁混合产生白烟,且丙为18电子分子,则丙为HCl,丁为NH3,若乙为氯气,其水溶液中含有HClO,具有漂白作用,故B正确;
C.若甲、丙、戊含有同一种元素,当甲为S,乙为氧气,丙为二氧化硫,丁为HClO等具有强氧化性的物质,戊为硫酸,则含S元素的化合价由低到高的顺序为甲<丙<戊,故C正确;
D.甲为短周期中原子半径最大的主族元素的单质,戊为碱,则甲为Na,乙为氧气,二者反应生成的丙可能为Na2O2或Na2O,故D错误;
故选D.
点评 本题考查无机物的推断,熟悉物质的性质及转化关系图中的反应是解答本题的关键,注意选项D为解答的难点,符合甲、丙、戊中同种元素的化合价升高为非金属元素或变价金属元素,题目难度较大.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
18. 某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2ΝΗ3(g)+CO2(g)
某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2ΝΗ3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
①不可以判断该分解反应已经达到平衡的是AD.
A.v正(NH3)=2v逆(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时的分解平衡常数:K=1.6×10-8(mol•L-1)3.
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量将增加(填“增加”、“减少”或“不变”).
④氨基甲酸铵分解反应的焓变△H>0(填“>”、“=”或“<”),熵变△S>0(填“>”、“=”或“<”).
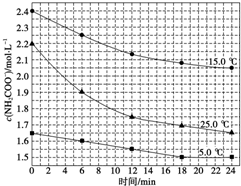
(2)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O,该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间的变化趋势如图所示.
⑤计算25.0℃时,0~6min氨基甲酸铵水解反应的平均速率:0.05mol/(L•min).
 某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2ΝΗ3(g)+CO2(g)
某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2ΝΗ3(g)+CO2(g)实验测得不同温度下的平衡数据列于下表:
| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总 浓度/mol•L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 | 9.4×10-3 |
A.v正(NH3)=2v逆(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时的分解平衡常数:K=1.6×10-8(mol•L-1)3.
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量将增加(填“增加”、“减少”或“不变”).
④氨基甲酸铵分解反应的焓变△H>0(填“>”、“=”或“<”),熵变△S>0(填“>”、“=”或“<”).
(2)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O,该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间的变化趋势如图所示.
⑤计算25.0℃时,0~6min氨基甲酸铵水解反应的平均速率:0.05mol/(L•min).
19.已知反应:
①2C(s)+O2(g)═2CO(g)△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol
下列结论正确的是( )
①2C(s)+O2(g)═2CO(g)△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol
下列结论正确的是( )
| A. | 碳的燃烧热110.5 kJ/mol | |
| B. | ①的反应热为221 kJ/mol | |
| C. | 稀醋酸与稀NaOH溶液反应的中和热为57.3kJ/mol | |
| D. | 稀盐酸与稀NaOH溶液反应的中和热为57.3kJ/mol |
16.在一定条件下化学反应:2SO2(g)+O2(g)═2SO3(g)△H=-197kJ/mol 现有容积相同且固定不变的甲、乙、丙三个容器,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列:
根据以上数据,下列叙述不正确的是( )
| 容器 | SO2(mol) | O2(mol) | N2(mol) | Q(kJ) |
| 甲 | 2 | 1 | 0 | Q1 |
| 乙 | 1 | 0.5 | 0 | Q2 |
| 丙 | 1 | 0.5 | 1 | Q3 |
| A. | Q2=Q3<98.5kJ | |
| B. | Q1=2Q2=2Q3=197kJ | |
| C. | 2Q2=2Q3<Q1<197kJ | |
| D. | 在上述条件下反应生成1molSO3气体放热98.5kJ |
3.设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 常温时56g铁片投入足量浓硫酸中生成NA个SO2分子 | |
| B. | 12g石墨和C60的混合物中质子总数一定为6NA个 | |
| C. | 25℃,pH=12的Na2CO3溶液中含有CO32-的数目为0.01NA | |
| D. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
13.我国规定食盐的含碘量(按每千克食盐含碘元素计)为20~40mg/Kg,则每千克食盐中加入碘酸钾的物质的量应不少于(设碘酸钾的摩尔质量为M g/mol)( )
| A. | $\frac{20×1{0}^{-3}}{127}$mol | B. | 20M mol | C. | $\frac{20×1{0}^{-3}}{M}$mol | D. | $\frac{20}{M}$mol |
20.如果1g O2中含有x个氧分子,则阿伏加德罗常数是( )
| A. | 32 x | B. | 32 x mol-1 | C. | 16 x | D. | 16 x mol-1 |
17.纯水在80℃时的pH( )
| A. | 等于7 | B. | 大于7 | C. | 小于7 | D. | 无法确定 |
