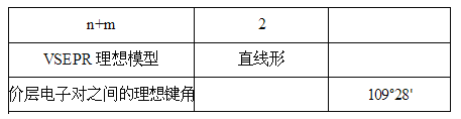
题目内容
【题目】亚硝酰氯(ClNO)是有机物合成中的重要试剂,可由NO与Cl2在常温常压下反应得到。ClNO部分性质如下:黄色气体,熔点:-59.6℃,沸点:-6.4℃,遇水易水解。已知:HNO2既有氧化性又有还原性;AgNO2微溶于水,能溶于硝酸:AgNO2+HNO3= AgNO3+ HNO2。
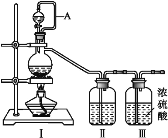
(1)利用Ⅰ、Ⅱ、Ⅲ装置制备原料气NO和Cl2
① 写出利用装置Ⅰ制备氯气的离子反应方程式:_________。
② 利用上述装置制备NO时,Ⅱ中盛装物质为_________(写化学式)。
(2)利用以下装置在常温常压下制备ClNO

① 装置连接顺序为a→________(按气流自左向右方向,用小写字母表示)。
② 为使NO和Cl2恰好完全反应生成ClNO,理论上通入NO和Cl2两种气体的流速比为_________。
③ 装置Ⅸ的作用是_____________。
④ 装置Ⅷ吸收尾气时,有同学认为尾气中的某种气体不能完全被吸收,为了充分吸收尾气,可将尾气与______________(气体)同时通入NaOH溶液中。
⑤ 王水是浓盐酸和浓硝酸的混酸,一定条件下混酸可生成ClNO和Cl2,该反应的化学方程式为______________________________________。
⑥ 写出验证ClNO与H2O完全反应后的溶液中存在Cl-和HNO2的实验步骤:取少量反应后的溶液于试管中,______________________________________________________。(限选试剂如下:AgNO3溶液,稀硝酸,KMnO4溶液)
【答案】MnO2+4H++2Cl-![]() Mn2+ + Cl2↑+2H2O H2O a→e→f→c→b→d (或a→f→e→c→b→d) 2∶1 冷凝亚硝酰氯,便于收集 O2(或空气) HNO3(浓)+3HCl(浓)=ClNO↑+Cl2↑+2H2O 依次滴加足量的AgNO3溶液和稀硝酸,充分振荡、静置,有白色沉淀生成;另取静置后上层清液少许于另一支试管中,滴加KMnO4溶液,溶液紫色褪去
Mn2+ + Cl2↑+2H2O H2O a→e→f→c→b→d (或a→f→e→c→b→d) 2∶1 冷凝亚硝酰氯,便于收集 O2(或空气) HNO3(浓)+3HCl(浓)=ClNO↑+Cl2↑+2H2O 依次滴加足量的AgNO3溶液和稀硝酸,充分振荡、静置,有白色沉淀生成;另取静置后上层清液少许于另一支试管中,滴加KMnO4溶液,溶液紫色褪去
【解析】
(1)、①制备氯气的离子反应方程式:MnO2+4H++2Cl-![]() Mn2+ + Cl2↑+2H2O;
Mn2+ + Cl2↑+2H2O;
②实验室收集NO只能用排水法,选择试剂H2O;
(2)、①ClNO易与水反应,装置VII可以防止尾气吸收装置VIII的水蒸气进入,所以连接顺序为a→e→f→c→b→d;
②由反应2NO+Cl2=2ClNO可知理论上通入NO和Cl2两种气体的流速比为2:1时恰好完全反应生成ClNO;
③ 由于ClNO沸点:-6.4℃,所以需要冰盐(-10℃)冷凝亚硝酰氯,才便于收集;
④空气中氧气与NO反应生成NO2,同时通入NaOH溶液中被NaOH溶液吸收,避免NO逸出污染空气;
⑤王水是浓盐酸和浓硝酸的混酸,一定条件下混酸可生成ClNO和Cl2,根据得失电子守恒和原子守恒,该反应的化学方程式为:HNO3(浓)+3HCl(浓)=ClNO↑+Cl2↑+2H2O;
⑥验证ClNO与H2O完全反应后的溶液中存在Cl-和HNO2,可根据Cl-与Ag+反应生成白色沉淀及HNO2具有还原性进行判断,具体操作为:依次滴加足量的AgNO3溶液和稀硝酸,充分振荡、静置,有白色沉淀生成;另取静置后上层清液少许于另一支试管中,滴加KMnO4溶液,溶液紫色褪去。