题目内容
【题目】两种金属组成的合金25克与氯气完全反应,共用去标况下氯气11.2升,该合金的可能组成是
A.Na和MgB.Cu和CaC.Cu和ZnD.Fe和Mg
【答案】B
【解析】
根据n=![]() 可知11.2L氯气的物质的量为n(Cl2)=
可知11.2L氯气的物质的量为n(Cl2)=![]() mol=0.5mol,金属与氯气反应时,氯元素由0价降为-1价,消耗氯气0.5mol,则转移电子0.5mol×2=1mol,由题意25g合金转移1mol电子;可用极值法进行判断,即消耗0.5mol氯气需要单一金属的质量,两种金属的质量必须满足一个大于25g,一个小于25g;
mol=0.5mol,金属与氯气反应时,氯元素由0价降为-1价,消耗氯气0.5mol,则转移电子0.5mol×2=1mol,由题意25g合金转移1mol电子;可用极值法进行判断,即消耗0.5mol氯气需要单一金属的质量,两种金属的质量必须满足一个大于25g,一个小于25g;
A. 1mol钠与氯气反应生成氯化钠,转移1mol电子需要1mol钠即23g;1mol镁24g与氯气反应生成氯化镁,转移2mol电子,转移1mol电子需要12g镁,转移1mol电子所需的钠和镁的质量均小于25g,该合金的组合不可能,故A错误;
B. 1mol铜64g与氯气反应生成氯化铜,转移2mol电子,转移1mol电子需要32g铜;1mol钙40g与氯气反应生成氯化钙,转移2mol电子,转移1mol电子需要20g钙,转移1mol电子所需的铜和钙的质量一个大于25g,一个小于25g,该合金的组合是可能的,故B正确;
C. 1mol铜64g与氯气反应生成氯化铜,转移2mol电子,转移1mol电子需要32g铜;1mol锌65g与氯气反应生成氯化锌,转移2mol电子,转移1mol电子需要32.5g锌,转移1mol电子所需的铜和锌的质量都大于25g,该合金的组合是不可能的,故C错误;
D. 1mol铁56g与氯气反应生成氯化铁,转移3mol电子,转移1mol电子需要约为18.7g铁;1mol镁24g与氯气反应生成氯化镁,转移2mol电子,转移1mol电子需要12g镁,转移1mol电子所需的铁和镁的质量都小于25g,该合金的组合是不可能的,故D错误;
答案选B。

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案【题目】
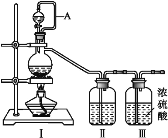
(一) 现代铝的精炼研究方向是减低能耗。如图 :室温下通过电解在阴极沉积纯铝,A1Br3 在苯(简写 ArH)中可以生成[A12Br5ArH]+和 Br-。
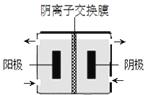
(1)阳极的材料________;
(2)写出阴极沉积铝的电极方程式__________________________________________;
(二)邻硝基苯甲酸是重要的医院中间体,最新合成方法是邻硝基甲苯和高锰酸钾在相转移催化剂季铵盐(Q+X-)氧化、酸化合成,其原理如下:
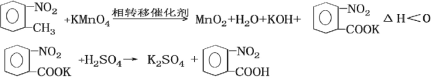
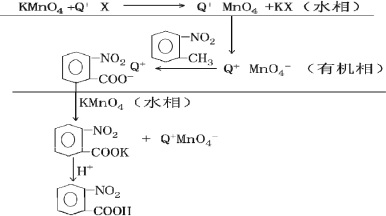
相转移催化原理如下:
有关物质的物理性质如下表:
物质 | 邻硝基苯甲酸 | 高锰酸钾 | 苄基三乙基氯化铵(C6H5-CH2CH2)N(C2H5)3Cl | 聚乙二醇 | 四丁基溴化铵(C4H9)4NBr | NH4Cl |
水 | 难溶 | 易溶 | 可溶 | 任意比互溶溶 | 可溶 | 易溶 |
有机物 | 易溶 | 难溶 | 易溶 | 易溶 | 易溶 | 难溶 |
下列说法不合理的是________;
A.相转移催化剂作用主要决定于 Q+的物理化学性质
B.反应中为了防止温度剧烈升高,投料应该分批加入
C.Q+X-是通过增大反应接触面积提高反应速率
D.增大压强可以提高邻硝基甲苯氧化的反应限度
E.工业使用季铵盐(Q+X-)可以提高邻硝基苯甲酸产率
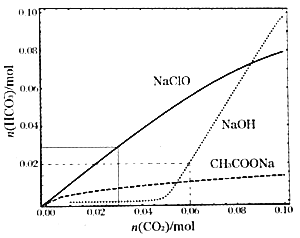
(2)四丁基溴化铵(C4H9)4NBr 萃取水中的高锰酸钾的方程式为:KMnO4(aq) +Q+X-(aq) →Q+ MnO4- (aq) +KX(aq),写出平衡常数 k 的表达式________________;设n(Q+X-):n(邻硝基甲苯)=x,理论证明当 x=5%邻硝基甲酸产率 y 得到最大值,请画出 y 随 x 变化的示意图________________ 。
(3)实验表明,当温度 100℃、反应时间 2.5h,n(KMnO4): n(邻硝基甲苯)=3:1,催化剂用量相同,Q+X-反应的催化效果如下:
相转移催化剂 | 苄基三乙基氯化铵 (C6H5-CH2CH2) N(C2H5)3Cl | 聚乙二醇 | 四丁基溴化铵 (C4H9)4NBr |
产率% | 46.7 | 20.0 | 53.1 |
苄基三乙基氯化铵比四丁基溴化铵催化效果差的原因_____________________________;工业生产不用聚乙二醇做催化剂的主要原因____________________________________ ;
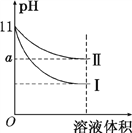
(4)(C4H9)4NBr 为催化剂,邻硝基甲苯和高锰酸钾反应,测得溶液酸碱性对产率、反应时间影响如图 ,下列推测合理的是________。

A.溶液碱性强产率降低是因为季铵盐发生水解反应
B.pH=2 高锰酸钾一定发生副反应
C.选择 pH=7、适当升温可以提高产率
D.工业可以选择浓硝酸替代高锰酸钾做氧化剂,减缓对设备的腐蚀