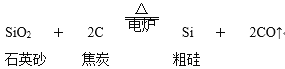
题目内容
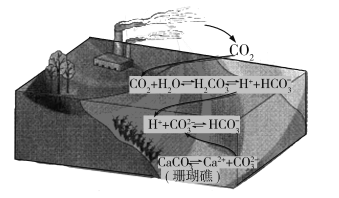
【题目】天然气的主要成分为CH4,一般还含有C2H6等烃类,是重要的燃料和化工原料。
(1)乙烷在一定条件可发生如下反应:C2H6(g)= C2H4(g)+H2(g) ΔH,相关物质的燃烧热数据如下表所示:
物质 | C2H6(g) | C2H4(g) | H2(g) |
燃烧热ΔH/( kJ·mol1) | -1560 | -1411 | -286 |
①ΔH=_________kJ·mol1。
②提高该反应平衡转化率的方法有_________、_________。
③容器中通入等物质的量的乙烷和氢气,在等压下(p)发生上述反应,乙烷的平衡转化率为α。反应的平衡常数Kp=_________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)高温下,甲烷生成乙烷的反应如下:2CH4![]() C2H6+H2。反应在初期阶段的速率方程为:r=k×
C2H6+H2。反应在初期阶段的速率方程为:r=k×![]() ,其中k为反应速率常数。
,其中k为反应速率常数。
①设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=_____ r1。
②对于处于初期阶段的该反应,下列说法正确的是_________。
A.增加甲烷浓度,r增大 B.增加H2浓度,r增大
C.乙烷的生成速率逐渐增大 D.降低反应温度,k减小
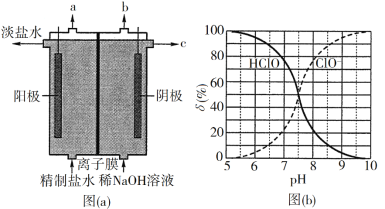
(3)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:
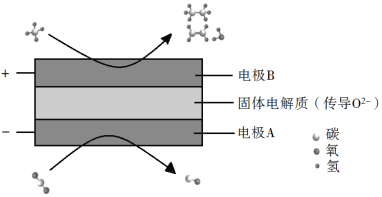
①阴极上的反应式为_________。
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH4和CO2体积比为_________。
【答案】137 升高温度 减小压强(增大体积) ![]() 1-α AD CO2+2e=CO+O2 6∶5
1-α AD CO2+2e=CO+O2 6∶5
【解析】
(1) ①先写出三种气体的燃烧热的热化学方程式,然后根据盖斯定律进行计算,得到目标反应的H;
②反应C2H6(g)![]() C2H4(g) + H2(g)为气体体积增大的吸热反应,升高温度、减小压强平衡等都向正反应方向移动;
C2H4(g) + H2(g)为气体体积增大的吸热反应,升高温度、减小压强平衡等都向正反应方向移动;
③根据已知乙烷的转化率,设起始时加入的乙烷和氢气各为1mol,列出三段式,求出平衡时各物质的分压,带入平衡常数的计算公式进行计算;
(2) ①根据r=k×![]() ,若r1=kc,甲烷转化率为
,若r1=kc,甲烷转化率为![]() 甲烷的浓度为c(1-
甲烷的浓度为c(1-![]() ),则r2= kc(1-
),则r2= kc(1-![]() );
);
②根据反应初期的速率方程为:r=k×![]() ,其中k为反应速率常数,据此分析速率变化的影响因素;
,其中k为反应速率常数,据此分析速率变化的影响因素;
(3) ①由图可知,CO2在阴极得电子发生还原反应,电解质传到O2-,据此写出电极反应;
②令生成乙烯和乙烷分别为2体积和1体积,根据阿伏加德罗定律,同温同压下,气体体积比等于物质的量之比,再根据得失电子守恒,得到发生的总反应,进而计算出为消耗CH4和CO2的体积比。
(1)①由表中燃烧热数值可知:
①C2H6(g)+![]() O2(g)=2CO2(g) +3H2O(l) H1= -1560kJmol-1;②C2H4(g)+3O2(g)=2CO2(g) +2H2O(l) H2= -1411kJmol-1;③H2(g)+
O2(g)=2CO2(g) +3H2O(l) H1= -1560kJmol-1;②C2H4(g)+3O2(g)=2CO2(g) +2H2O(l) H2= -1411kJmol-1;③H2(g)+![]() O2(g)=H2O(l) H3= -286kJmol-1;根据盖斯定律可知,①-②-③得C2H6(g) =C2H4(g) + H2(g),则H= H1-H2-H3=( -1560kJmol-1)-( -1411kJmol-1)- ( -286kJmol-1)=137kJmol-1,故答案为137;
O2(g)=H2O(l) H3= -286kJmol-1;根据盖斯定律可知,①-②-③得C2H6(g) =C2H4(g) + H2(g),则H= H1-H2-H3=( -1560kJmol-1)-( -1411kJmol-1)- ( -286kJmol-1)=137kJmol-1,故答案为137;
②反应C2H6(g) ![]() C2H4(g) + H2(g)为气体体积增大的吸热反应,升高温度、减小压强平衡都向正反应方向移动,故提高该反应平衡转化率的方法有升高温度、减小压强(增大体积);
C2H4(g) + H2(g)为气体体积增大的吸热反应,升高温度、减小压强平衡都向正反应方向移动,故提高该反应平衡转化率的方法有升高温度、减小压强(增大体积);
③设起始时加入的乙烷和氢气各为1mol,列出三段式,
C2H6(g) ![]() C2H4(g) + H2(g)
C2H4(g) + H2(g)
起始(mol) 1 0 1
转化(mol) ![]() α α
α α
平衡(mol) 1-![]()
![]() 1+
1+![]()
平衡时,C2H6![]() p、
p、![]() p和
p和![]() p,则反应的平衡常数为Kp=
p,则反应的平衡常数为Kp=![]() ;
;
(2) ①根据r=k×![]() ,若r1= kc,甲烷转化率为
,若r1= kc,甲烷转化率为![]() 甲烷的浓度为c(1-
甲烷的浓度为c(1-![]() ),则r2= kc(1-
),则r2= kc(1-![]() ),所以r2=(1-
),所以r2=(1-![]() )r1;
)r1;
②A.增大反应物浓度反应速率增大,故A说法正确;
B.由速率方程可知,初期阶段的反应速率与氢气浓度无关,故B说法错误;
C.反应物甲烷的浓度逐渐减小,结合速率方程可知,乙烷的生成速率逐渐减小,故C说法错误;
D.化学反应速率与温度有关,温度降低,反应速率常数减小,故D正确。
答案选AD。
(3) ①由图可知,CO2在阴极得电子发生还原反应,电极反应为CO2+2e-=CO+O2-;
②令生成乙烯和乙烷分别为2体积和1体积,根据阿伏加德罗定律,同温同压下,气体体积比等于物质的量之比,再根据得失电子守恒,得到发生的总反应为:6CH4+5CO2=2C2H4+ C2H6+5H2O+5CO,即消耗CH4和CO2的体积比为6:5。故答案为:6:5。

 计算高手系列答案
计算高手系列答案【题目】已知:①(![]() +HNO3
+HNO3![]()
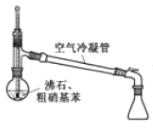
![]() +H2O △H<0;②硝基苯沸点210.9℃,蒸馏时选用空气冷凝管。下列制取硝基苯的操作或装置(部分夹持仪器略去),正确的是
+H2O △H<0;②硝基苯沸点210.9℃,蒸馏时选用空气冷凝管。下列制取硝基苯的操作或装置(部分夹持仪器略去),正确的是
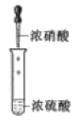
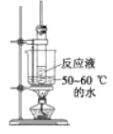
选项 | A | B | C | D |
装置 |
|
|
|
|
目的 | 分液 | 配制混酸 | 水浴加热 | 蒸馏提纯 |
A.AB.BC.CD.D