题目内容
13.在下列物质中:①Cu ②S ③KNO3 ④FeCl3溶液 ⑤SO3 ⑥蔗糖 ⑦CH4⑧熔融NaCl ⑨HCl ⑩Ba(OH)2
属于电解质的是③⑧⑨⑩,属于非电解质的是⑤⑥⑦,能导电的是①④⑧.
分析 能导电的物质中含有自由移动的阴阳离子或电子,如金属或电解质溶液能导电;
在水溶液里或熔融状态下能导电的化合物是电解质,酸、碱、盐、金属氧化物都属于电解质;
在水溶液里和熔融状态下都不导电的化合物是非电解质,非金属氧化物、部分非金属氢化物和大多数有机物属于非电解质;
单质和混合物既不是电解质也不是非电解质.
解答 解::①Cu是单质,含有自由电子,能导电;属于单质,既不是电解质也不是非电解质;
②S不含有自由移动的阴阳离子或电子,不导电;属于单质,既不是电解质也不是非电解质;
③KNO3 不含有自由移动的阴阳离子或电子,不导电;在水溶液里或熔融状态下能导电的化合物是电解质;
④FeCl3溶液含有自由移动的阴阳离子,能够导电;属于混合物,既不是电解质也不是非电解质;
⑤SO3 不含有自由移动的阴阳离子或电子,不导电;本身不能电离产生自由移动离子,属于非电解质;
⑥蔗糖不含有自由移动的阴阳离子或电子,不导电;在水溶液里和熔融状态下都不导电的化合物是非电解质;
⑦CH4不含有自由移动的阴阳离子或电子,不导电;在水溶液里和熔融状态下都不导电的化合物是非电解质;
⑧熔融NaCl含有自由移动的阴阳离子,能够导电;在水溶液里或熔融状态下能导电的化合物是电解质;
⑨HCl 不含有自由移动的阴阳离子或电子,不导电;在水溶液里能导电的化合物是电解质;
⑩Ba(OH)2不含有自由移动的阴阳离子或电子,不导电;在水溶液里或熔融状态下能导电的化合物是电解质;
所以:属于电解质的是:③⑧⑨⑩;属于非电解质的是:⑤⑥⑦;能导电的是:①④⑧;
故答案为:③⑧⑨⑩、⑤⑥⑦、①④⑧.
点评 本题考查了物质的导电性、电解质和非电解质的判断,明确物质导电的原因与电解质和非电解质的关系是解本题关键,注意导电的不一定是电解质.

 作业辅导系列答案
作业辅导系列答案(1)造气阶段的反应为:CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.1kJ/mol
①在一密闭容器中进行上述反应,测得 CH4的物质的量浓度随反应时间的变化如下图1所示.反应中处于平衡状态的时间为5~10min、12min后;10min时,改变的外界条件可能是升高温度.
②如图2所示,在初始容积相等的甲、乙两容器中分别充入等物质的量的CH4和H2O.在相同温度下发生反应,并维持反应过程中温度不变.则达到平衡时,两容器中CH4的转化率大小关系为:α甲(CH4)<α乙(CH4);
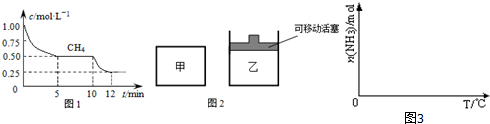
(2)转化阶段发生的可逆反应为:CO(g)+H2O(g)?CO2(g)+H2(g)
一定温度下,反应的平衡常数为K=1.某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
(3)合成氨反应为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol?1
①依据温度对合成氨反应的影响,在图3坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图.
②根据勒夏特列原理,简述提高合成氨原料转化率的一种方法增大压强或降低温度或分离液氨.
(4)工业合成氨的热化学方程式为
N2(g)+3H2(g)?2NH3(g),△H=-92.4kJ•mol-1.
在某压强恒定的密闭容器中加入2mol N2和4mol H2,达到平衡时,N2的转化率为50%,体积变为10L.求:
①该条件下的平衡常数为400;
②若向该容器中加入a mol N2、b mol H2、c mol NH3,且a、b、c均大于0,在相同条件下达到平衡时,混合物中各组分的物质的量与上述平衡相同.反应放出的热量<(填“>”“<”或“=”)92.4kJ.
| A. | 氢氧化铁与足量的氢碘酸溶液反应:Fe(OH)3+3H+=Fe3++3H2O | |
| B. | 硫酸亚铁溶液中加入过氧化氢溶液:2Fe2++H2O2+2H+=2Fe3++2H2O | |
| C. | NaHCO3溶液中加入少量石灰水:HCO3-+Ca2++OH-=CaCO3↓+H2O | |
| D. | 向NaAlO2溶液中通入足量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
 ,该物质分子中所含的官能团有氨基、羧基(填写名称).
,该物质分子中所含的官能团有氨基、羧基(填写名称).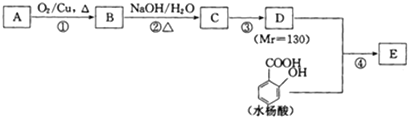

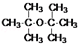 .
.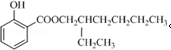 .
.