题目内容
【题目】一定温度下,某密闭的真空容器中加入足量的碳酸钙,发生反应CaCO3(s)![]() CaO(s)+CO2(g),达到平衡,下列说法正确的是( )
CaO(s)+CO2(g),达到平衡,下列说法正确的是( )
A.将体积缩小为原来的一半,当体系再次达到平衡时,CO2的压强不变
B.该反应的△H<0
C.将碳酸钙粉碎进行反应可以提高碳酸钙的转化率
D.保持压强不变,充入He,再次达到平衡时,CaO的质量减少
【答案】A
【解析】
对于反应CaCO3(s)![]() CaO(s)+CO2(g),为吸热反应,K=c(CO2),温度不变,则c(CO2)不变,容器内气体的密度不变,以此解答该题。
CaO(s)+CO2(g),为吸热反应,K=c(CO2),温度不变,则c(CO2)不变,容器内气体的密度不变,以此解答该题。
A、由于温度不变,则平衡常数K=c(CO2)不变,将体积缩小为原来的一半,当体系再次达到平衡时,CO2的浓度不变,故A正确;
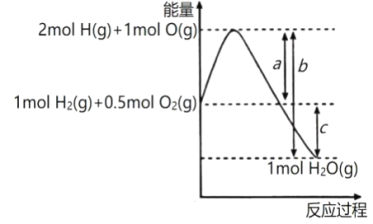
B、因CaCO3(s)需持续加热才能分解为CaO(s)、CO2(g),故该反应为吸热反应,因此△H>0,故B错误;
C、将碳酸钙粉碎进行反应,只能够提高化学反应速率,化学平衡不移动,因此不能改变其转化率,故C错误;
D、保持容器压强不变,充入He,则体积增大,CO2浓度减小,平衡正向移动,再次达到平衡时,CaO的质量增加,故D错误;
故答案为A。

【题目】工业上制取CuCl2的生产流程如下:
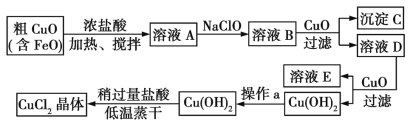
请结合下表数据,回答问题:
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
溶度积(25 ℃) | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
(1)在溶液A中加入NaClO的目的是________________________。
(2)在溶液B中加入CuO的作用是________________________________。
(3)操作a的目的是__________________________。
(4)在Cu(OH)2中加入盐酸使Cu(OH)2转化为CuCl2,采用稍过量盐酸和低温蒸干的目的是________________。