题目内容
19.下列化合物中只有离子键的是( )| A. | MgCl2 | B. | Na2O2 | C. | KHSO4 | D. | NH4Cl |
分析 活泼金属和活泼非金属元素易形成离子键,非金属元素之间易形成共价键,部分碱、大多数盐、金属氧化物、铵盐中都含有离子键,据此分析解答.
解答 解:A.氯化镁中镁离子和氯离子之间只存在离子键,为离子化合物,故A正确;
B.过氧化钠中钠离子和过氧根离子之间存在离子键、O-O原子之间存在共价键,属于离子化合物,故B错误;
C.硫酸氢钾中钠离子和硫酸氢根离子之间存在离子键、H-0和S-O原子之间存在共价键,所以离子化合物,故C错误;
D.氯化铵中铵根离子和氯离子之间存在离子键、N-H原子之间存在共价键,故D错误;
故选A.
点评 本题考查离子键和共价键的判断,侧重考查基本概念,明确物质的构成微粒及微粒之间作用力即可解答,注意不能根据是否含有金属元素判断离子键,易错选项是D.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列叙述I和II均正确并有因果关系的是( )
| 选项 | 叙述I | 叙述II |
| A | 晶体硅熔点高硬度大 | 可用于制作半导体材料 |
| B | BaSO4难溶于酸 | 用硫酸和BaCl2溶液检验SO42- |
| C | NH3极易溶于水 | NH3可用于设计喷泉实验 |
| D | NaOH可以与SiO2反应 | 用NaOH溶液雕刻工艺玻璃上的纹饰 |
| A. | A | B. | B | C. | C | D. | D |
7.关于硫原子核外电子的叙述错误的是( )
| A. | 排布在K、L、M三个电子层上 | B. | 3p能级上有2个空轨道 | ||
| C. | 共有16种不同的运动状态 | D. | 共有5种不同的能级 |
14.炼铁的还原剂CO是由焦炭和CO2反应而得.现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)?2CO(g)△H=Q kJ/mol.如图为CO2、CO的物质的量n随时间t的变化关系图.下列说法正确的是( )
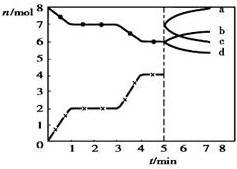

| A. | 1~3min时,v(CO)=v(CO2) | |
| B. | 当容器内的压强不变时,该反应一定达到平衡状态,且$\frac{P(平衡)}{P(开始)}<1$ | |
| C. | 若3min时温度由T1升高到T2,则Q>O,且$\frac{K({T}_{2})}{K({T}_{1})}$=4.7 | |
| D. | 5min时再充入一定量的CO,c、b曲线分别表示n(CO)、n(CO2)的变化 |
4.物质结构决定性质,深入研究物质的微观结构,有利于理解物质变化的本质.请回答下列问题:
(1)C、Si、N的电负性由大到小的顺序是N>C>Si;C、N、O、F的第一电离能由大到小的顺序是F>N>O>C.
(2)A、B均为短周期金属元素.依据表中的数据,写出B原子的电子排布式:1s22s22p63s2.
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关.一般而言,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色.据此判断,[Mn(H2O)6]2+有颜色(填“无”或“有”).
(4)L的原子核外电子占有9个轨道,而且有一个未成对电子,L是Cl(填元素符号).
(1)C、Si、N的电负性由大到小的顺序是N>C>Si;C、N、O、F的第一电离能由大到小的顺序是F>N>O>C.
(2)A、B均为短周期金属元素.依据表中的数据,写出B原子的电子排布式:1s22s22p63s2.
| 电离能/(kJ•mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
(4)L的原子核外电子占有9个轨道,而且有一个未成对电子,L是Cl(填元素符号).
8.一定条件下,H2O2在水溶液中发生分解反应:2H2O2 $\frac{\underline{\;一定条件\;}}{\;}$2H2O+O2↑,反应过程中,测得不同时间H2O2的物质的量浓度如下表:
(1)H2O2的分解反应是氧化还原反应(填“是”或“不是”).
(2)该分解反应0─20min的平均反应速率v(H2O2)为0.02mol•L-1min-1.
(3)如果反应所用的H2O2溶液为100mL,则0─80min共产生O2Cg.
A.0.08 B.0.16 C.1.2 D.2.4.
| t/min | 0 | 20 | 40 | 60 | 80 |
| c(H2O2)/mol•L-1 | 0.80 | 0.40 | 0.20 | 0.10 | 0.05 |
(2)该分解反应0─20min的平均反应速率v(H2O2)为0.02mol•L-1min-1.
(3)如果反应所用的H2O2溶液为100mL,则0─80min共产生O2Cg.
A.0.08 B.0.16 C.1.2 D.2.4.
9.某芳香烃的分子式为C10H14,不能使溴水褪色,分子结构中只含有一个侧链烃基,则此侧链烃基的结构共有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |