题目内容
8.一定条件下,H2O2在水溶液中发生分解反应:2H2O2 $\frac{\underline{\;一定条件\;}}{\;}$2H2O+O2↑,反应过程中,测得不同时间H2O2的物质的量浓度如下表:| t/min | 0 | 20 | 40 | 60 | 80 |
| c(H2O2)/mol•L-1 | 0.80 | 0.40 | 0.20 | 0.10 | 0.05 |
(2)该分解反应0─20min的平均反应速率v(H2O2)为0.02mol•L-1min-1.
(3)如果反应所用的H2O2溶液为100mL,则0─80min共产生O2Cg.
A.0.08 B.0.16 C.1.2 D.2.4.
分析 (1)有电子转移的化学反应是氧化还原反应,其特征是有元素化合价升降;
(2)v(H2O2)=$\frac{△c}{△t}$;
(3)0─80min内消耗n(H2O2)=(0.80-0.08)mol/L×0.1L=0.075mol,根据双氧水和氧气的关系式计算氧气物质的量,再根据m=nM计算氧气质量.
解答 解:(1)有电子转移的化学反应是氧化还原反应,其特征是有元素化合价升降,该反应中O元素化合价由-1价变为0价、-2价,所以有电子转移,为氧化还原反应,
故答案为:是;
(2)v(H2O2)=$\frac{△c}{△t}$=$\frac{(0.80-0.40)mol/L}{(20-0)min}$=0.02mol/(L.min),
故答案为:0.02;
(3)0─80min内消耗n(H2O2)=(0.80-0.05)mol/L×0.1L=0.075mol,根据双氧水和氧气的关系式得n(O2)=$\frac{1}{2}$n(H2O2)=0.0375mol,氧气质量m=nM=0.0375mol×32g/mol=1.2g,
故选C.
点评 本题考查氧化还原反应判断、根据方程式的计算、化学反应速率计算等基本计算、概念,侧重考查学生分析计算能力,注意氧化还原反应本质和特征区别,题目难度不大.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
19.下列化合物中只有离子键的是( )
| A. | MgCl2 | B. | Na2O2 | C. | KHSO4 | D. | NH4Cl |
3.氯化钠是日常生活中人们常用的调味品.下列性质可以证明氯化钠中一定存在离子键的是( )
| A. | 常温下能溶于水 | B. | 水溶液能导电 | C. | 具有较高的熔点 | D. | 熔融状态能导电 |
13.下列说法错误的是( )
| A. | NH4+和CH4属于等电子体,立体构型都是正四面体 | |
| B. | 主族元素的原子核外电子最后填入的能级是s能级或p能级 | |
| C. | BF3、NCl3、H2O分子中所有原子都满足最外层为8电子结构的是NCl3 | |
| D. | 向盛有硫酸铜溶液的试管里加入过量氨水,将得到蓝色的氢氧化铜沉淀 |
20.化学式为C8H16O2的有机物A在酸性条件下能水解生成C和D,且C在一定条件下能转化为D,则有机物A的结构可能有( )
| A. | 1 种 | B. | 2 种 | C. | 3 种 | D. | 4 种 |
17.下列试剂:①浓氨水 ②氯水 ③硝酸银 ④浓硝酸 ⑤浓盐酸 ⑥溴化银,其中必须用棕色试剂瓶盛装的有( )
| A. | ①②③④⑤⑥ | B. | ②③④⑥ | C. | ②③⑤⑥ | D. | ①③④⑤ |
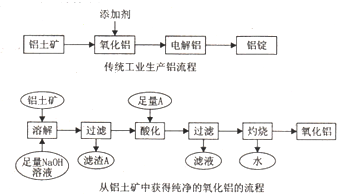
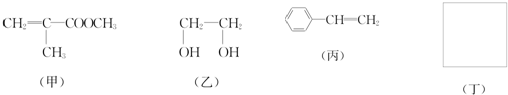
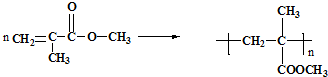
 利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是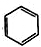 +CH3CH2Cl$→_{△}^{AlCl_{3}}$
+CH3CH2Cl$→_{△}^{AlCl_{3}}$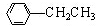 +HCl.
+HCl.