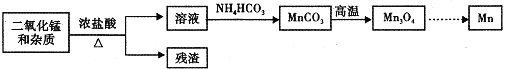
题目内容
【题目】正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4℃,密度比水小。某实验小组利用如下装置合成正丁醚(其它装置均略去),发生的主要反应为:2C3CH2CH2CH2OH![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
实验过程如下:在容积为100mL的三颈烧瓶中将5mL浓硫酸、14.8g正丁醇和几粒沸石混合均匀,再加热回流一段时间,收集到粗产品,精制得到正丁醚.回答下列问题:

(1)合成粗产品时,液体试剂加入顺序是___________________.
(2)实验中冷凝水应从__________口出去(填“a”或“b”).
(3)为保证反应温度恒定在135℃,装置C中所盛液体必须具有的物理性质为___________.
(4)加热时间过长或温度过高,反应混合液会变黑,写出用NaOH溶液吸收有毒尾气的离子方程式__________.
(5)得到的正丁醚粗产品依次用8mL 50%的硫酸、10mL水萃取洗涤.该步骤中需要的属于硅酸盐材质的实验仪器是烧杯、玻璃棒、_____________.该仪器使用前需要_______________________.
(6)将分离出的有机层用无水氯化钙干燥,过滤后再进行___________(填操作名称)精制得到正丁醚.
(7)本实验最终得到6.50g正丁醚,则正丁醚的产率是_________.
【答案】先加正丁醇,后加浓硫酸 a 该液体沸点大于135℃ 2OH-+SO2=SO32-+H2O 分液漏斗 检漏 蒸馏 50.0%
【解析】
(1)因浓硫酸密度较大,一般浓硫酸与其它液体混合时,先加其它液体后加硫酸;
(2)用冷凝管冷凝时,为了充分冷却,采用逆流的方法,即冷凝水的流向与气体流向相反;
(3)液体能达到的最高温度等于其沸点,装置C中所盛液体必须点大于135℃;
(4)分离分层的液体用分液漏斗;带有玻璃塞的仪器使用前要检漏;
(5)有机物易挥发,将分离出的有机层用无水氯化钙干燥,过滤后再进行蒸馏,精制得到正丁醚;
(6)产率= ![]() ×100%。
×100%。
(1)浓硫酸与其它液体混合时,先加其它液体后加硫酸,防止浓硫酸稀释时放热,引起液体飞溅,所以液体试剂加入顺序是先加正丁醇,后加浓硫酸;
故答案为:先加正丁醇,后加浓硫酸;
(2)用冷凝管冷凝时,冷凝水的流向与气体流向相反,则冷凝水从a口进入;
故答案为:a;
(3)加热液体能达到的最高温度等于其沸点,则为保证反应温度恒定在135℃,装置C中所盛液体的沸点应该大于135℃;
故答案为:该液体沸点大于135℃;
(4)加热时间过长或温度过高,反应混合液会变黑,浓硫酸与丁醇发生氧化还原反应,浓硫酸被还原生成二氧化硫,用氢氧化钠溶液吸收二氧化硫,其二氧化硫与氢氧化钠的反应离子方程式为:2OH-+SO2═SO32-+H2O;
故答案为:2OH-+SO2═SO32-+H2O;
(5)分离分层的液体用分液漏斗,该步骤中需要的属于硅酸盐材质的实验仪器是烧杯、玻璃棒、分液漏斗;带有玻璃塞的仪器使用前要检漏,则在使用分液漏斗时要先检验是否漏水;
故答案为:分液漏斗;检验是否漏水;
(6)将分离出的有机层用无水氯化钙干燥,正丁醚易挥发,采用蒸馏的方法获得纯净的正丁醚;
故答案为:蒸馏;
(7)由2CH3CH2CH2CH2OH![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O,
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O,
74×2 130
14.8g mg
则m=![]() =13.0g,产率=
=13.0g,产率=![]() ×100%=
×100%=![]() ×100%=50.0%;
×100%=50.0%;
故答案为50.0%。

【题目】已知下列物质在 20 ℃下的 Ksp 如下,试回答下列问题:
化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
Ksp | 2.0×10-10 | 5.4×10-13 | 8.3×10-17 | 2.0×10-48 | 2.0×10-12 |
(1)20 ℃时,上述五种银盐饱和溶液中,Ag+物质的量浓度由大到小的顺序是_______(用化学式表示)。
(2)向等浓度的 KCl 和 KBr 的混合溶液中逐渐加入 AgNO3 溶液,当两种沉淀共存时,![]() =__________。
=__________。
(3)测定水中 Cl-含量时,常用 Ag+进行滴定,滴定时,应加入的指示剂是_____。
A.KBr B.KI C.K2S D.K2CrO4