��Ŀ����
����Ŀ����֪���������� 20 ���µ� Ksp ���£��Իش��������⣺
��ѧʽ | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
��ɫ | ��ɫ | dz��ɫ | ��ɫ | ��ɫ | ��ɫ |
Ksp | 2.0��10-10 | 5.4��10-13 | 8.3��10-17 | 2.0��10-48 | 2.0��10-12 |
��1��20 ��ʱ�������������α�����Һ�У�Ag�����ʵ���Ũ���ɴ�С��˳����_______���û�ѧʽ��ʾ����
��2�����Ũ�ȵ� KCl �� KBr �Ļ����Һ������ AgNO3 ��Һ�������ֳ�������ʱ��![]() ��__________��
��__________��
��3���ⶨˮ�� Cl-����ʱ������ Ag�����еζ����ζ�ʱ��Ӧ�����ָʾ����_____��
A��KBr B��KI C��K2S D��K2CrO4
���𰸡�Ag2CrO4��AgCl��AgBr��AgI��Ag2S 3.7��102 D
��������
(1)AgCl��AgBr��AgI������Һ��c(Ag+)=![]() ��Ag2S��Ag2CrO4������Һ��c(Ag+)=
��Ag2S��Ag2CrO4������Һ��c(Ag+)=![]() ��
��
(2)��Ũ�Ⱦ�Ϊ0.1mol/L��KCl��KBr�����Һ�м�������AgNO3��Һ�������ֳ�������ʱ��![]() =
=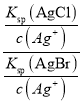 =
=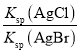 ��
��
(3)�ⶨˮ�����Ȼ��ﺬ�������ñ������������еζ����ζ�ʱӦ�����ָʾ���������ӷ�Ӧ�������ӷ�Ӧ��
(1)AgCl��AgBr��AgI������Һ��c(Ag+)=![]() �����������������ܶȻ�����֪��c(Ag+)��AgCl��AgBr��AgI��AgCl��Һ��c(Ag+)��1.4��10-5mol/L��AgBr��Һ��c(Ag+)��0.7��10-6mol/L��AgI��Һ��c(Ag+)��0.9��10-8mol/L��Ag2S��Ag2CrO4������Һ��c(Ag+)=
�����������������ܶȻ�����֪��c(Ag+)��AgCl��AgBr��AgI��AgCl��Һ��c(Ag+)��1.4��10-5mol/L��AgBr��Һ��c(Ag+)��0.7��10-6mol/L��AgI��Һ��c(Ag+)��0.9��10-8mol/L��Ag2S��Ag2CrO4������Һ��c(Ag+)=![]() �������ܶȻ�����֪��Ag2CrO4��Һ��c(Ag+)=
�������ܶȻ�����֪��Ag2CrO4��Һ��c(Ag+)=![]() ��1.6��10-4mol/L��Ag2S��Һ��c(Ag+)��1.6��10-16mol/L�����������������α�����Һ�У�c(Ag+)�ɴ�С��˳���ǣ�Ag2CrO4��AgCl��AgBr��AgI��Ag2S��
��1.6��10-4mol/L��Ag2S��Һ��c(Ag+)��1.6��10-16mol/L�����������������α�����Һ�У�c(Ag+)�ɴ�С��˳���ǣ�Ag2CrO4��AgCl��AgBr��AgI��Ag2S��
(2)��Ũ�Ⱦ�Ϊ0.1mol/L��KCl��KBr�����Һ�м�������AgNO3��Һ�������ֳ�������ʱ![]() =
=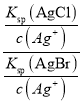 =
=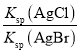 =
=![]() =3.7��102��
=3.7��102��
(3)�ⶨˮ�����Ȼ��ﺬ�������ñ������������еζ����ζ�ʱӦ�����ָʾ���������ӷ�Ӧ�������ӷ�Ӧ����(1)֪��Ӧ�ü���K2CrO4���ʴ�Ϊ��D��

 ��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�����Ŀ��ij�¶��£� ��ӦH2(g)+CO2(g)![]() H2O(g)+CO(g)��ƽ�ⳣ��
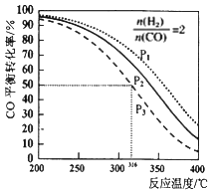
H2O(g)+CO(g)��ƽ�ⳣ��![]() �����¶����������Ϊ10 L�������ܱ������зֱ���뷴Ӧ���ʼ��������ͼ��ʾ�������жϲ���ȷ����
�����¶����������Ϊ10 L�������ܱ������зֱ���뷴Ӧ���ʼ��������ͼ��ʾ�������жϲ���ȷ����
��ʼ�� | �� | �� | �� |
H2 ��mol�� | 1 | 2 | 2 |
CO2��mol�� | 1 | 1 | 2 |
A.��Ӧ��ʼʱ�����еķ�Ӧ�������������еķ�Ӧ�������
B.ƽ��ʱ���ͱ���CO2��ת������ȣ�����60��
C.ƽ��ʱ,���У�2��ת���ʴ���60%
D.ƽ��ʱ�����У�(��2 ) ��0. 08 mol��L-1
����Ŀ���ϳɼ״��ķ�Ӧ2H2(g)+CO(g)![]() CH3OH(g) ��H= -90.8kJ��t���´˷�Ӧ��ƽ�ⳣ��Ϊ160�����¶��£����ܱ������п�ʼֻ����CO��H2����Ӧl0min���ø���ֵ�Ũ�����£�
CH3OH(g) ��H= -90.8kJ��t���´˷�Ӧ��ƽ�ⳣ��Ϊ160�����¶��£����ܱ������п�ʼֻ����CO��H2����Ӧl0min���ø���ֵ�Ũ�����£�
���� | H2 | CO | CH3OH |
Ũ��(mol/L) | 0.2 | 0.1 | 0.4 |
(1)д���÷�Ӧ��ƽ�ⳣ������ʽK=___________________��
(2)��ʱ����ڷ�Ӧ����v(H2)=______________��
(3)�Ƚϴ�ʱ�����淴Ӧ���ʵĴ�С��v�� ___v��(����>������<������=��)
(4)��Ӧ�ﵽƽ����������������䣬�����������������һ����v��_____(����������������С������������)��v��______(����������������С������������),ƽ����____(����������������������������)�ƶ���ƽ�ⳣ��K____(����������������С������������)��
����Ŀ��25 ��ʱ��������������Һ��
�� | �� | �� | �� |
0.1 mol��L��1��ˮ | pH��11��ˮ | 0.1 mol��L��1���� | pH��3���� |
����˵������ȷ����(����)
A. ��ϡ�͵�ԭ����100����pH�����ͬ
B. ������٢ۻ�ϡ�������ڢܻ�����õ���Һ��������
C. �٢��зֱ��������CH3COONa���壬![]() ��ֵ����С
��ֵ����С
D. �ۢ�ϡ�͵�ԭ����100����ϡ�ͺ����Һ�е�pH��