题目内容
15.下列实验装置通常不用于物质分离提纯的是( )| A. | 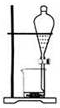 | B. | 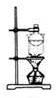 | C. | 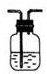 | D. | 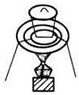 |
分析 A.分液用于分离分层的液体混合物;
B.升华用于固体混合物分离;
C.洗气用于混合气体的分离;
D.为固体分解或测定结晶水的实验.
解答 解:A中分液、B中升华、C中洗气均为常见的混合物分离提纯方法,只有D加热坩埚,不能用于物质分离提纯,
故选D.
点评 本题考查混合物分离提纯实验装置,为高频考点,把握实验装置的作用、常见混合物分离方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
8.铁与铝的混合物共16.4g,与700mL盐酸恰好完全反应,在标况下,共收集到15.68L的氢气.下列说法错误的是( )
| A. | 氢气的物质的量为0.7mol | B. | 铁的物质的量为0.1mol | ||
| C. | 铝的物质的量为0.2mol | D. | 盐酸浓度为2mol/L |
9.某物质R与水和氧气发生反应的化学方程式为:2R+2H2O+7O2=2FeSO4+2H2SO4,推断R的化学式为( )
| A. | FeS | B. | FeS2 | C. | FeO | D. | Fe2S3 |
5.许多化学物质都是一柄“双刃剑”,请仿照例子,说出下列物质的功与过.
| 物质的化学式 | 功 | 过 |
| 例:CO2 | 固态CO2(干冰)可用于人工降雨 | 空气中CO2含量过高造成温室效应 |
| O2 | ||
| H2 |
7.一种有机镁化合物X可用于制造防毒布料的涂布液,它可吸收空气中的甲醛,其反应原理如图(已配平):
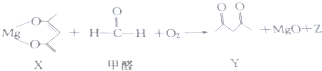
下列有关该反应的说法正确的是( )
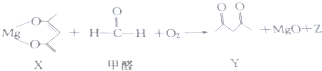
下列有关该反应的说法正确的是( )
| A. | Z的结构式为O-C-O | B. | X是还原剂 | ||
| C. | 甲醛是氧化剂 | D. | 除去1mol甲醛时,转移4mol电子 |
 Cu(OH)2·CuCl2+2HCl↑+2H2O↑。则下列有关叙述中错误的是( )
Cu(OH)2·CuCl2+2HCl↑+2H2O↑。则下列有关叙述中错误的是( )