题目内容
3.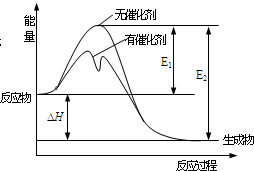 2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A. | 该反应为吸热反应 | |
| B. | 升高温度,不影响活化分子百分数 | |
| C. | 使用催化剂使该反应的反应热发生改变 | |
| D. | E1-E2=△H |
分析 A.图象分析反应物能量高于生成物能量,反应是放热反应;
B.升高温度,活化分子百分数增大,单位体积内的活化分子数增大;
C.催化剂对反应的焓变无影响;
D.图象分析反应焓变=E1-E2.
解答 解:A.图象分析反应物能量高于生成物能量,反应是放热反应,故A错误;
B.升高温度,活化分子百分数增大,单位体积内的活化分子数增大,所以反应速率增大,故B错误;
C.催化剂对反应的始态和状态无响应,只改变活化能,则对反应的焓变无影响,故C错误;
D.△H=断键吸收的能量-成键放出的能量=E1-E2,故D正确.
故选D.
点评 本题考查了化学变化过程中能量变化的分析的,主要是活化能概念的理解应用,掌握图象分析方法是关键,题目较简单.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
13.下列溶液中有关物质的量浓度关系正确的是( )
| A. | 0.1 mol•L-1NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| B. | 0.1 mol•L-1NaHCO3溶液与0.1 mol•L-1NaOH溶液等体积混合:c(Na+)=2c(CO32-)+c(HCO3-)+2c(H2CO3) | |
| C. | 0.1 mol•L-1NaHCO3溶液与0.2 mol•L-1NaOH溶液等体积混合:c(Na+)>c(OH-)>0.05 mol•L-1>c(CO32-)>c(HCO3-) | |
| D. | 0.2 mol•L-1NaHCO3溶液与0.1 mol•L-1NaOH溶液等体积混合:c(CO32-)+c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+) |
14.下列反应中前者属于取代反应,后者属于加成反应的是( )
| A. | 甲烷与氯气混合后光照反应;乙烯使酸性高锰酸钾溶液褪色 | |
| B. | 乙烯与溴的四氯化碳溶液反应;苯与氢气在一定条件下反应生成环己烷 | |
| C. | 苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成; 乙烯与水生成乙醇的反应 | |
| D. | 在苯中滴入溴水,溴水褪色;乙烯自身生成聚乙烯的反应 |
11.以下是处于研究阶段的“人工固氮”的新方法.N2在催化剂表面与水发生反应:2N2(g)+6H2O(l)?4NH3(g)+3O2(g)△H=+1530.4kJ/mol;完成下列填空:
(1)上述反应在高温(填高温、低温、任何温度)下能自发进行.
(2)该反应平衡常数K的表达式K=$\frac{{c}^{4}(N{H}_{3})•{c}^{3}({O}_{2})}{{c}^{2}({N}_{2})}$.
(3)上述反应达到平衡后,保持其他条件不变,升高温度,重新达到平衡,则ac.
a.平衡常数K增大 b.H2O的浓度减小 c.容器内的压强增大 d.v逆(O2)减小
(4)研究小组分别在四个容积为2升的密闭容器中,充入N2 1mol、H2O 3mol,在催化剂条件下进行反应3小时.实验数据见表:
第四组实验中以NH3表示反应的速率是33×10-7mol/L•h,与前三组相比,NH3 生成量最小的原因可能是催化剂在80℃活性减小,反应速率反而减慢.
(5)氨水是实验室常用的弱碱.
①往CaCl2溶液中通入CO2至饱和,无明显现象.再通入一定量的NH3后产生白色沉淀,此时溶液中一定有的溶质是NH4Cl.请用电离平衡理论解释上述实验现象饱和H2CO3溶液中电离产生的CO32-很少,因此没有沉淀,加入氨水后,促进H2CO3的电离,CO32-离子浓度增大,有沉淀产生.
②向盐酸中滴加氨水过量至溶液呈中性,则离子浓度的关系是c(NH4+)>c(OH-)>c(Cl-)>c(H+).
(1)上述反应在高温(填高温、低温、任何温度)下能自发进行.
(2)该反应平衡常数K的表达式K=$\frac{{c}^{4}(N{H}_{3})•{c}^{3}({O}_{2})}{{c}^{2}({N}_{2})}$.
(3)上述反应达到平衡后,保持其他条件不变,升高温度,重新达到平衡,则ac.
a.平衡常数K增大 b.H2O的浓度减小 c.容器内的压强增大 d.v逆(O2)减小
(4)研究小组分别在四个容积为2升的密闭容器中,充入N2 1mol、H2O 3mol,在催化剂条件下进行反应3小时.实验数据见表:
| 序号 | 第一组 | 第二组 | 第三组 | 第四组 |
| t/℃ | 30 | 40 | 50 | 80 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
(5)氨水是实验室常用的弱碱.
①往CaCl2溶液中通入CO2至饱和,无明显现象.再通入一定量的NH3后产生白色沉淀,此时溶液中一定有的溶质是NH4Cl.请用电离平衡理论解释上述实验现象饱和H2CO3溶液中电离产生的CO32-很少,因此没有沉淀,加入氨水后,促进H2CO3的电离,CO32-离子浓度增大,有沉淀产生.
②向盐酸中滴加氨水过量至溶液呈中性,则离子浓度的关系是c(NH4+)>c(OH-)>c(Cl-)>c(H+).
18.短周期元素X、Y、Z、W在元素周期表中的位置如表所示,其中X所处的周期序数与主族序数之和为8.下列说法错误的是( )
| X | Y | ||
| Z | W |
| A. | W的原子半径最大 | |
| B. | Z与X形成的化合物难溶于水 | |
| C. | Y的单质不能与水反应 | |
| D. | Z元素的氧化物对应水化物的酸性一定弱于W的氧化物对应水化物的酸性 |
8.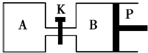 如图所示的装置中发生反应2A2(g)+B2(g)?2C(g)△H=-a kJ/mol(a>0),已知P是可自由滑动的活塞.在相同温度时关闭K,向容积相同的A、B容器中分别都充入2mol A2和1mol B2气体.两容器分别在500℃达平衡时,A中C的浓度为c1 mol/L,放出热量b kJ,B中C的浓度为c2 mol/L,放出热量c kJ.下列说法中正确的是( )
如图所示的装置中发生反应2A2(g)+B2(g)?2C(g)△H=-a kJ/mol(a>0),已知P是可自由滑动的活塞.在相同温度时关闭K,向容积相同的A、B容器中分别都充入2mol A2和1mol B2气体.两容器分别在500℃达平衡时,A中C的浓度为c1 mol/L,放出热量b kJ,B中C的浓度为c2 mol/L,放出热量c kJ.下列说法中正确的是( )
 如图所示的装置中发生反应2A2(g)+B2(g)?2C(g)△H=-a kJ/mol(a>0),已知P是可自由滑动的活塞.在相同温度时关闭K,向容积相同的A、B容器中分别都充入2mol A2和1mol B2气体.两容器分别在500℃达平衡时,A中C的浓度为c1 mol/L,放出热量b kJ,B中C的浓度为c2 mol/L,放出热量c kJ.下列说法中正确的是( )
如图所示的装置中发生反应2A2(g)+B2(g)?2C(g)△H=-a kJ/mol(a>0),已知P是可自由滑动的活塞.在相同温度时关闭K,向容积相同的A、B容器中分别都充入2mol A2和1mol B2气体.两容器分别在500℃达平衡时,A中C的浓度为c1 mol/L,放出热量b kJ,B中C的浓度为c2 mol/L,放出热量c kJ.下列说法中正确的是( )| A. | 500℃达平衡时有:c1>c2 | |
| B. | 500℃达平衡时有:a>b>c | |
| C. | 达平衡后打开K,容器B的体积将减小 | |
| D. | 此反应的平衡常数随温度升高而增大 |
15.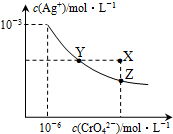 t℃时,AgCl的Ksp=2×10-10;Ag2CrO4是一种橙红色固体,在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
t℃时,AgCl的Ksp=2×10-10;Ag2CrO4是一种橙红色固体,在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
 t℃时,AgCl的Ksp=2×10-10;Ag2CrO4是一种橙红色固体,在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
t℃时,AgCl的Ksp=2×10-10;Ag2CrO4是一种橙红色固体,在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )| A. | 在t℃时,AgCl的溶解度大于Ag2CrO4 | |
| B. | 在t℃时,Ag2CrO4的Ksp=1×10-12 | |
| C. | 在饱和Ag2CrO4溶液中加入K2CrO4,可使溶液由Y点到X点 | |
| D. | 在t℃时,用AgNO3标准溶液滴定20mL未知浓度的KCl溶液,不能采用K2CrO4溶液为指示剂 |
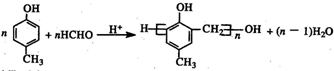
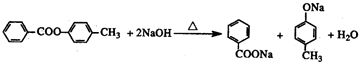
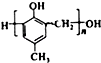 ,化合物C和化合物N的合成路线如下:
,化合物C和化合物N的合成路线如下: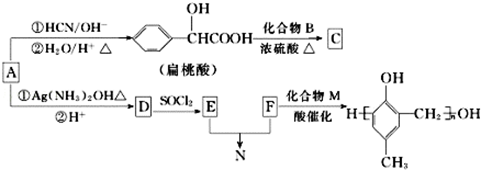
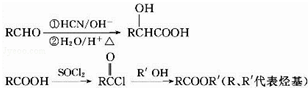
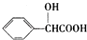
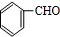 ,D的含氧官能团的名称是羧基.
,D的含氧官能团的名称是羧基.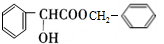 .
. .
. .
. )有多种同分异构体.其中含有三个取代基,能与FeCl3溶液发生显色反应,也能与NaHCO3溶液反应放出气体的同分异构体共有10种,写出符合条件的三个取代基不相邻的一种同分异构体的结构简式
)有多种同分异构体.其中含有三个取代基,能与FeCl3溶液发生显色反应,也能与NaHCO3溶液反应放出气体的同分异构体共有10种,写出符合条件的三个取代基不相邻的一种同分异构体的结构简式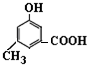 .
.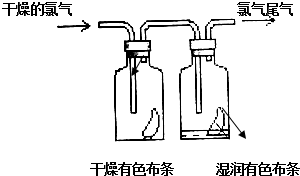 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有湿润有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有湿润有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.