题目内容
8.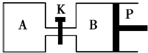 如图所示的装置中发生反应2A2(g)+B2(g)?2C(g)△H=-a kJ/mol(a>0),已知P是可自由滑动的活塞.在相同温度时关闭K,向容积相同的A、B容器中分别都充入2mol A2和1mol B2气体.两容器分别在500℃达平衡时,A中C的浓度为c1 mol/L,放出热量b kJ,B中C的浓度为c2 mol/L,放出热量c kJ.下列说法中正确的是( )
如图所示的装置中发生反应2A2(g)+B2(g)?2C(g)△H=-a kJ/mol(a>0),已知P是可自由滑动的活塞.在相同温度时关闭K,向容积相同的A、B容器中分别都充入2mol A2和1mol B2气体.两容器分别在500℃达平衡时,A中C的浓度为c1 mol/L,放出热量b kJ,B中C的浓度为c2 mol/L,放出热量c kJ.下列说法中正确的是( )| A. | 500℃达平衡时有:c1>c2 | |
| B. | 500℃达平衡时有:a>b>c | |
| C. | 达平衡后打开K,容器B的体积将减小 | |
| D. | 此反应的平衡常数随温度升高而增大 |
分析 A为恒容容器,B是恒压容器,反应2A2(g)+B2(g)?2C(g)发生以后,气体的物质的量之和减小,所以B相当于在A的基础上加压,所以平衡B对于A而言是加压了,向右移动,C的浓度增大,放出的热量增加,由此分析解答.
解答 解:A、平衡B对于A而言是加压了,向右移动,C的浓度增大,所以c1<c2,故A错误;
B、方程式中a是2mol A2和1mol B2气体完全反应,平衡B对于A而言是加压了,向右移动,C的浓度增大,放出的热量增加,所以a>c>b,故B错误;
C、打开K后,因为B端压强的大于A端的压强,所以B中压强会减小,活塞P会向左移动,故b的体积减小,故C正确;
D、正反应是放热反应,温度越高K值越小,故D错误;
故选:C.
点评 本题综合考查影响化学反应速率、化学平衡移动的因素以及化学平衡常数等知识,综合性强,难度大.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
18. N、O、Na、Mg、S、Br是常见的六种元素.
N、O、Na、Mg、S、Br是常见的六种元素.
(1)Br位于元素周期表第四周期第ⅦA族;基态Na+核外有10种运动状态不同的电子.Mg基态原子核外电子排布式为1s22s22p63s2.
(2)用“>”或“<”填空:
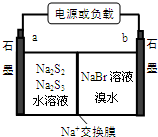
(3)已知多硫化钠-溴储能电池是一种二次电池,结构如图.电池总反应为:2Na2S3+2NaBr$?_{放电}^{充电}$3Na2S2+Br2
①放电时Na+向b极迁移(填“a或b”).
②充电时阴极电极反应式为:2S32-+2e-=3S22-.
(4)已知N4为正四面体结构,N-N键能为167kJ/mol,N≡N键能为942kJ/mol.写出N4(g)转化为N2(g)的热化学方程式N4(g)=2N2(g)△H=-882kJ/mol.
 N、O、Na、Mg、S、Br是常见的六种元素.
N、O、Na、Mg、S、Br是常见的六种元素.(1)Br位于元素周期表第四周期第ⅦA族;基态Na+核外有10种运动状态不同的电子.Mg基态原子核外电子排布式为1s22s22p63s2.
(2)用“>”或“<”填空:
| 第一电离能 | 粒子半径 | 熔点 | 键的极性 |
| N>S | S2->Mg2+ | SO3<Na2O2 | H-O<H-N |
①放电时Na+向b极迁移(填“a或b”).
②充电时阴极电极反应式为:2S32-+2e-=3S22-.
(4)已知N4为正四面体结构,N-N键能为167kJ/mol,N≡N键能为942kJ/mol.写出N4(g)转化为N2(g)的热化学方程式N4(g)=2N2(g)△H=-882kJ/mol.
19. 已知甲、乙、丙、丁是中学化学常见的物质,一定条件下可发生如图转化:下列相关离子方程式或化学方程式错误的是( )
已知甲、乙、丙、丁是中学化学常见的物质,一定条件下可发生如图转化:下列相关离子方程式或化学方程式错误的是( )
 已知甲、乙、丙、丁是中学化学常见的物质,一定条件下可发生如图转化:下列相关离子方程式或化学方程式错误的是( )
已知甲、乙、丙、丁是中学化学常见的物质,一定条件下可发生如图转化:下列相关离子方程式或化学方程式错误的是( )| A. | ①可能为CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | B. | ①可能为Fe+2Fe3+═3Fe2+ | ||
| C. | ②可能为2NO+O2═2NO2 | D. | ②可能为CO32-+H2O+CO2═2HCO3- |
16.如图仪器使用、操作或试剂保存正确的是( )
| A. |  移取醋酸 | B. | 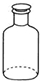 盛装NaOH溶液 | C. | 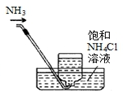 收集氨气 | D. | 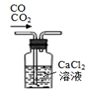 除去杂质CO2气体 |
3.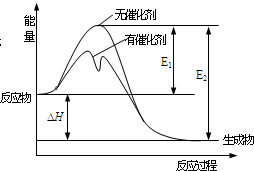 2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
 2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A. | 该反应为吸热反应 | |
| B. | 升高温度,不影响活化分子百分数 | |
| C. | 使用催化剂使该反应的反应热发生改变 | |
| D. | E1-E2=△H |
13.某有机物的结构简式如图所示,有关该有机物的叙述不正确的是( )
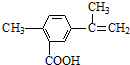

| A. | 在一定条件下,能发生取代、氧化、酯化和加聚反应 | |
| B. | 该物质分子中最多可以有9个碳原子在同一平面上 | |
| C. | 1 mol该物质最多可与4 mol H2发生加成反应 | |
| D. | 1 mol该物质完全氧化最多可消耗13 mol氧气 |
20.NA表示阿伏加德罗常数.下列说法正确的是( )
| A. | 7.8 g Na2O2中含有的阴离子数目为0.2NA | |
| B. | 标准状况下,2.24 L CHCl3的分子数为0.1NA | |
| C. | 1 L 0.1 mol/L Al2(SO4)3溶液中,Al3+的数目为0.2NA | |
| D. | 0.1 mol Fe与足量稀HNO3反应,转移电子数为0.3NA |
5.在恒温恒容条件下,可逆反应:A(s)+2B(g)?2C(g)+D(g)△H<0,在甲、乙、丙三个容器中建立平衡的相关信息如下表.则下列说法正确的是( )(Qc表示浓度熵)
| 容器 | 体积 | 起始物质 | 平衡时C的物质的量 | 平衡时B的体积分数 | 平衡常数 |
| 甲 | 1L | 1molA+2molB | 1mol | φ甲 | K甲 |
| 乙 | 1L | 4molC+2molD | n1 mol | φ乙 | K乙 |
| 丙 | 2L | 4molC+2molD | n2 mol | φ丙 | K丙 |
| A. | 在建立平衡的过程中,甲的Qc逐渐减小,乙和丙的Qc逐渐增大 | |
| B. | K甲=K丙>K乙 | |
| C. | 升高甲的温度,可使φ甲=φ乙 | |
| D. | n1=1.6,n2=2 |
6.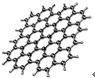 从石墨中分离出来的石墨烯是已知最薄、最坚硬的物质,可制成电阻率最小的纳米材料,其结构如图所示.下列关于石墨烯的说法正确的是( )
从石墨中分离出来的石墨烯是已知最薄、最坚硬的物质,可制成电阻率最小的纳米材料,其结构如图所示.下列关于石墨烯的说法正确的是( )
 从石墨中分离出来的石墨烯是已知最薄、最坚硬的物质,可制成电阻率最小的纳米材料,其结构如图所示.下列关于石墨烯的说法正确的是( )
从石墨中分离出来的石墨烯是已知最薄、最坚硬的物质,可制成电阻率最小的纳米材料,其结构如图所示.下列关于石墨烯的说法正确的是( )| A. | 具有良好的导电性 | B. | 属于高分子化合物 | ||
| C. | 与金刚石互为同位素 | D. | 不能与氧气发生反应 |